
Chemo therapie induzierte Kardio toxizität (CIC) bleibt eine große klinische Herausforderung bei der Behandlung von akuter myeloischer Leukämie (AML). Während Anthra cycline wie Daunorubicin (DNR) häufig als First-Line-Wirkstoffe eingesetzt werden, können ihre kardio toxischen Wirkungen-insbesondere bei pädiatrischen und jungen erwachsenen Patienten-die langfristige Herzfunktion und das Überleben beeinträchtigen.
Eine kürzlich von Prof. Hao Zhang und Dr. Yiwei Liu durchgeführte Studie, die im European Heart Journal (IF = 37,6) ver öffentlicht wurde, zeigt, wie IL-1α, das aus Tumorzellen freigesetzt wird, den Herz stoffwechsel stört. Beitrag zur Herz funktions störung während der Chemo therapie.
Diese Forschung hebt das inter zelluläre Übersprechen zwischen Tumor-und Herz zellen hervor und ident ifi ziert IL-1α als Schlüssel mediator. Entscheidend ist, dass die Studie zeigt, dass die Neutral isierung von IL-1α Herz verletzungen lindert, ohne die Wirksamkeit von Leukämie zu beeinträchtigen.
* Service Provider: Um zell spezifische Stoffwechsel veränderungen im Patienten gewebe zu untersuchen, wandte sich das Team anEinzelzellen-Sequenz ierungs dienste | 10x-Based-CRO-Omics Empower-Mit technischer Unterstützung vonOmics Empower.
Endo myokard biopsie proben wurden von einem repräsent ativen AML-Patienten entnommen, der kurz nach Erhalt einer DNR-basierten Chemo therapie eine Herz insuffizienz entwickelte. Zur Kontrolle wurde Gewebe von einem hirn toten Spender mit normaler Herzfunktion gewonnen.
Die Single-Nucleus-RNA-Sequenz ierung (snRNA-seq) wurde durchgeführt, um Transkript ions profile zu analysieren. Acht große Herz zelltypen wurden ident ifi ziert. Differential expressions analyze und Pseudozeit-Trajektorien-Rekonstruktion zeigten, dass eine Untergruppe von Kardiomyozyten beim AML-Patienten zeigteMetabolische Dys regulation, Gekennzeichnet durch:
Herunter regulierung von Genen im Zusammenhang mitFettsäure stoffwechsel
Upregulation von Genen, die an beteiligt sindGlukose stoffwechsel
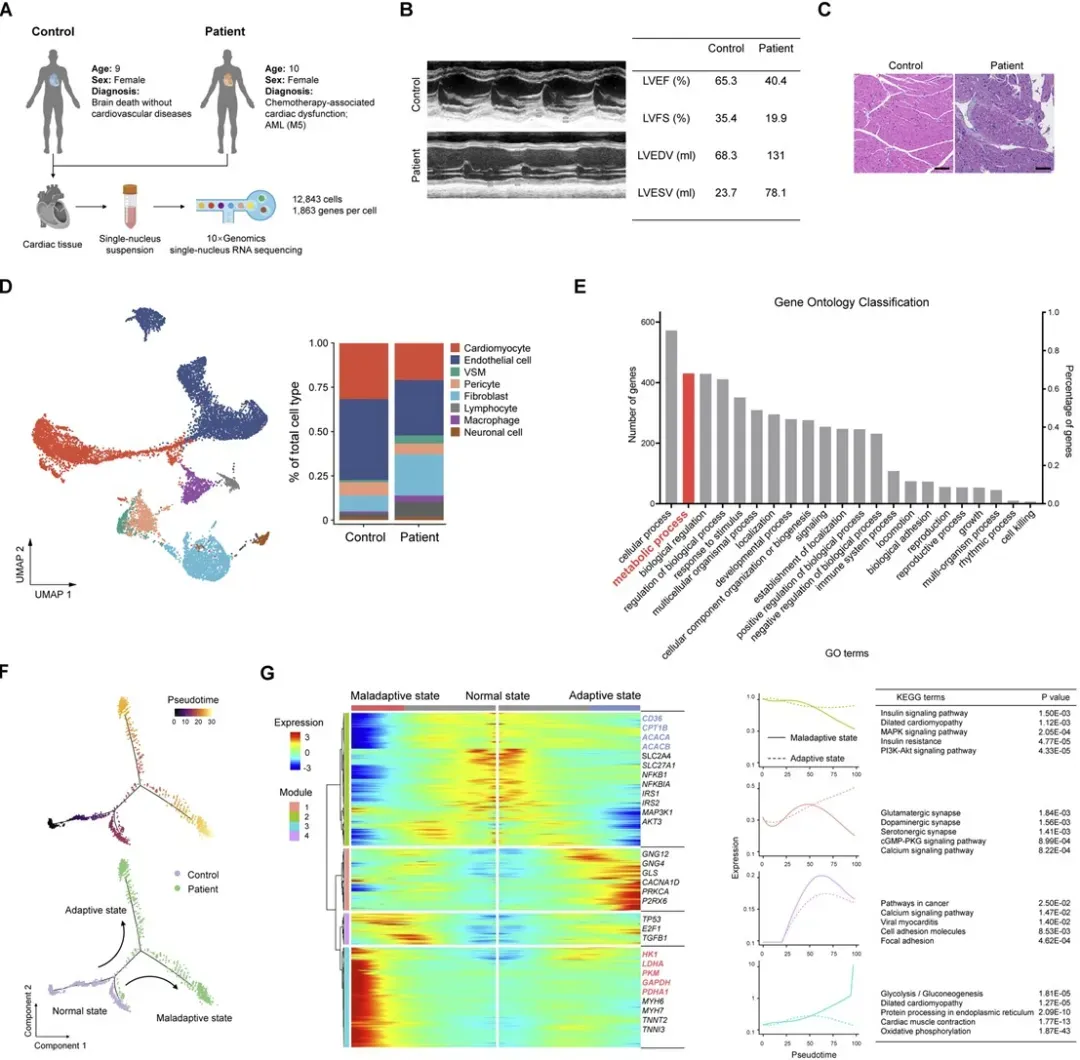
Abbildung 1. Herz metabolische Störung bei einem AML-Patienten nach Daunorubicin (DNR)-Behandlung
Um eine durch Chemo therapie induzierte Herzfunktion zu modellieren, haben die Forscher ein AML-Mausmodell erstellt. Folgende DNR-Verwaltung:
Mäuse ausgestelltHerz verletzungUnd verminderte Herzfunktion
Im Vergleich zu unbehandelten AML-Mäusen,Fettsäure-Aufnahme wurde deutlich reduziert, WährendDie Glukose aufnahme wurde erhöht
Diese Mäuse zeigten auch Anzeichen vonKardiale Energie mangel, Einschl ießlich:
Reduzierte ATP-Spiegel
Mitochondriale Schwellung und geringere Cristae-Dichte
Beeint rächt igte mitochondriale Atmung
Wichtig ist, dass diese Phänotypen warenNicht bei tumor freien (TF) Mäusen beobachtetBehandelt mit der gleichen Dosis von DNR, unter streicht die Rolle der Leukämie bei Herz-Stoffwechsel störungen.
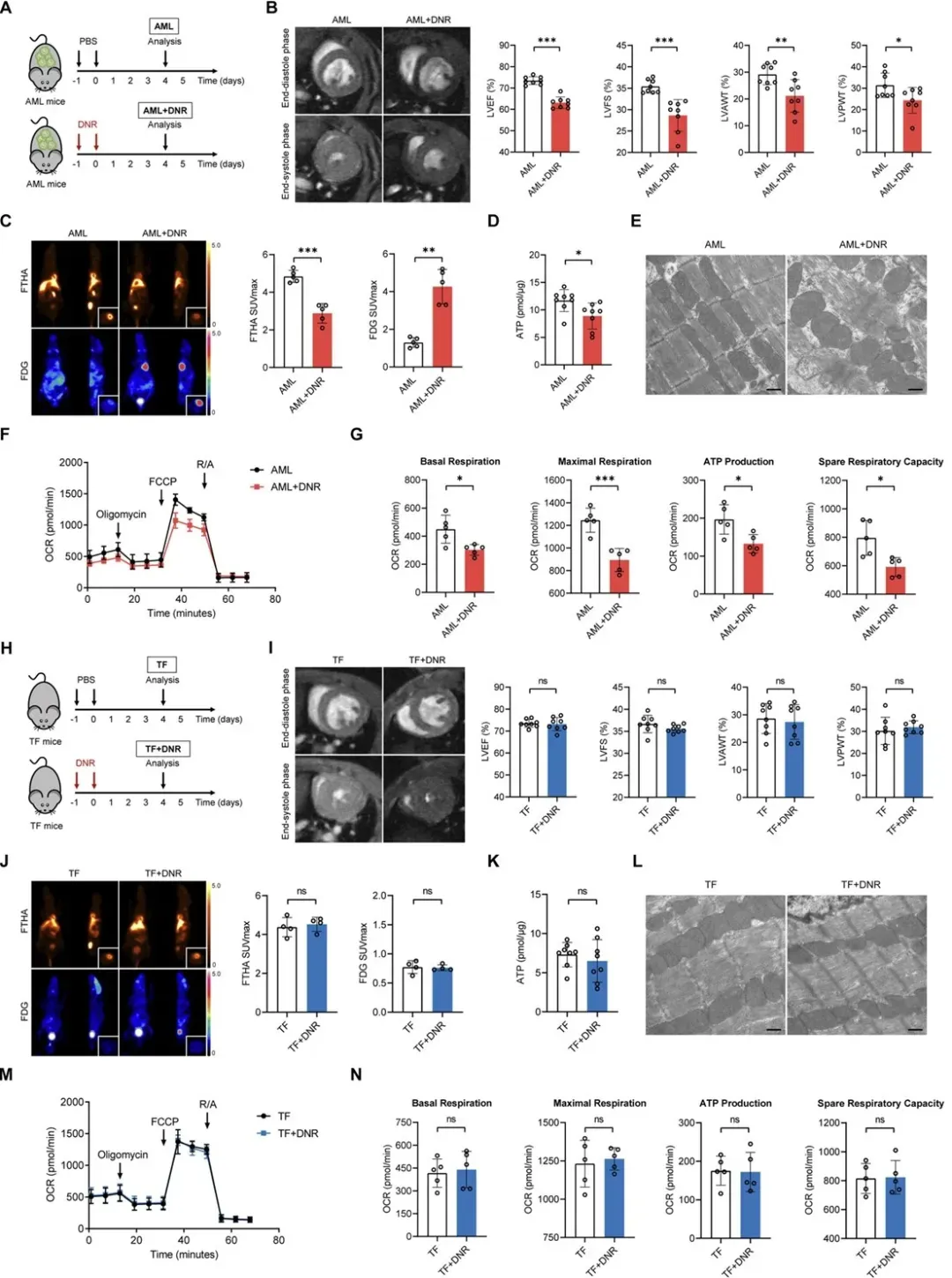
Abbildung 2. Herz-Stoffwechsel-Umbau und Funktions störung bei AML-Mäusen nach DNR-Behandlung
Um die Präferenz des Herz substrats während der Chemo therapie direkt zu untersuchen,Stabile Isotopen-markierte Stoffwechsel fluss analyzeWurde in AML-und AML-DNR-Mäusen durchgeführt. Die Daten enthüllten:
Eine bedeutendeVerringerung der Fettsäure oxidation
Erhöhte Glukose verwertungAls kompensator ische Antwort
Diese Verschiebung jedochHat die ATP-Produktion nicht vollständig wieder hergestellt
ZusatzaL Analyse zeigte erhöhten Fluss durchDer Pentose phosphat weg (PPP)Und verbesserter Glukose eintrag in dieTCA-ZyklusIn DNR-behandelten AML-Herzen.
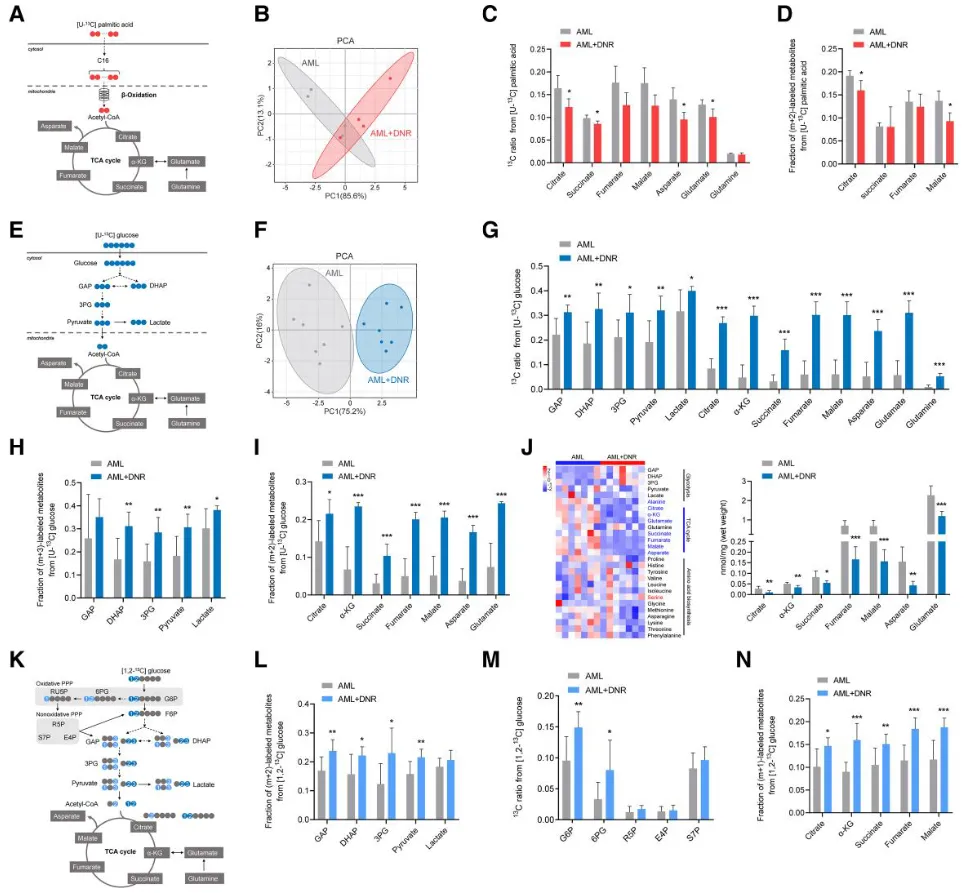
Abbildung 3. Die Isotopen verfolgung zeigt einen gestörten Fettsäure stoffwechsel bei DNR-behandelten AML-Mäusen
Bulk-RNA-seq schlug vor, dass die Zytokin-Signal übertragung zur beobachteten Stoffwechsel störung in AML-DNR-Maus herzen beitragen kann. Nachfolgende Proteomik-und Immun fluoreszenz analysen ident ifi ziertInterleukin-1 Alpha (IL-1α)Als Schlüssel faktor:
Die IL-1α-Proteins piegel waren bei AML-DNR-Mäusen (im Vergleich zu Kontrollen) signifikant erhöht.
Ähnliche Erhöhungen wurden im Herz gewebe von AML-Patienten beobachtet
In einer Patienten ko horte,Plasma-IL-1α-Spiegel korrelierten negativ mit der links ventrikulären Ejektion fraktion (LVEF)
Diese Ergebnisse legen nahe, dassTumor-abgeleitete IL-1α ist an einer chemo therapie assoziierten Herzfunktion störung beteiligt, Konsistent sowohl für Tiermodelle als auch für menschliche Proben.
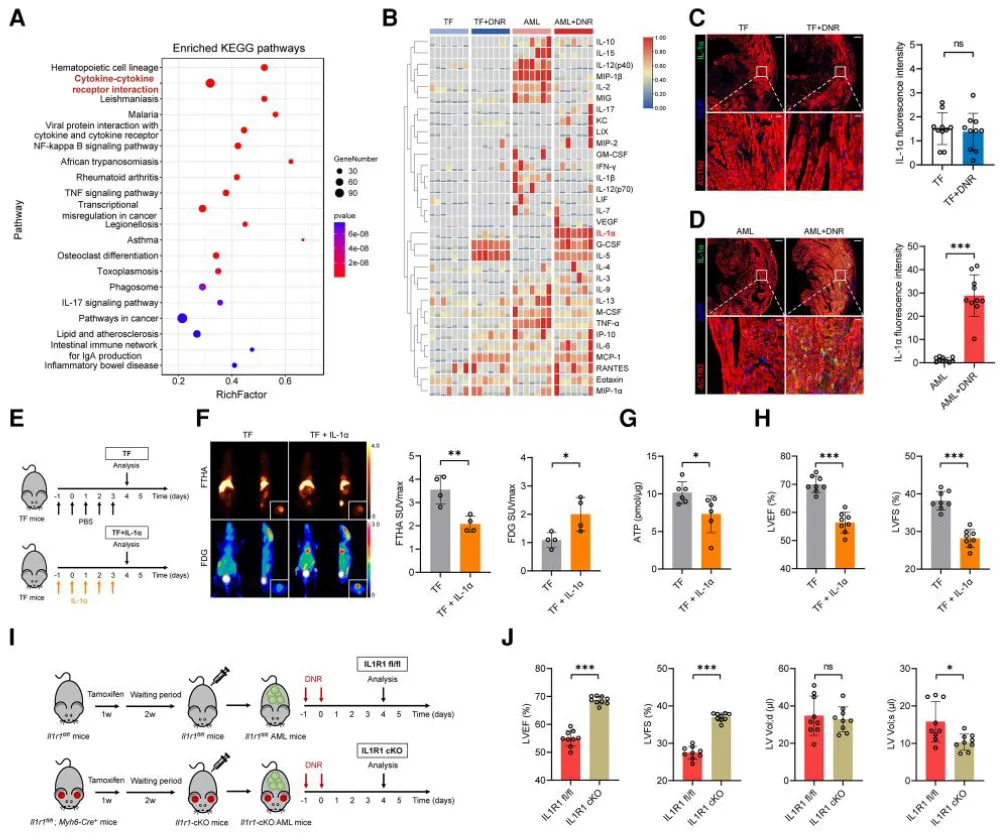
Abbildung 4. IL-1α vermittelt metabolische Dysfunktion im Herzen
Um die Quelle von IL-1α zu identifizieren, behandelten die Autoren THP-1 Leukämie zellen in vitro mit DNR. Durchfluss zytometrie, H & E-Färbung und Immun fluoreszenz bestätigten die Produktion und Freisetzung von IL-1α aus AML-Zellen nach der Chemo therapie.
In vivo verwendeten die Autoren Il1a-globale Knockout-Mäuse, die mit MLL-AF9 AML-Zellen transplant iert waren:
Die IL-1α-Protein expression im Herzen blieb bei Knockout-Mäusen unverändert
Die Herz funktions störung blieb nach der DNR bestehen, was darauf hindeutet, dassAML-Zellen-keine Wirtszellen-waren die dominierende Quelle von IL-1α
Weitere Experimente unter Verwendung von shIL-1α-transduzierten AML-Zellen zeigten:
Verbesserte Herzfunktion
Erhöhte myokard iale ATP-Spiegel
Reduzierte IL-1α-Färbung im Herz gewebe
Diese Ergebnisse verknüpfen direktChemo therapie induzierte IL-1α-Sekretion aus AML-ZellenZu einer Herz verletzung.
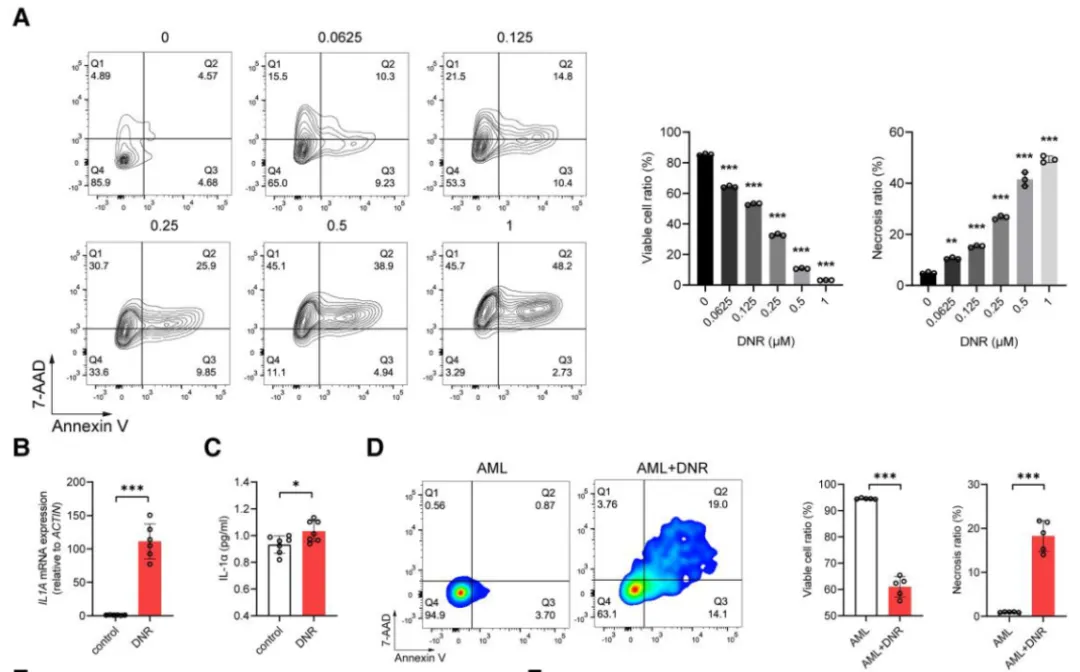
Abbildung 5. AML-Zellen setzen IL-1α als Reaktion auf die DNR-Behandlung frei
VerwendungIngenuity Pathway Analyse (IPA)Und PPI-Netzwerk analyze von Herz transkript omen schlugen die Autoren vor, dassIL-1α aktiviert NF-κB, Die wiederumUnterdrückt PGC-1α, Ein wichtiger Transkript ions regulator des Fettsäure stoffwechsels und der Mitochondrien funktion.
Western Blot und RT-PCR bestätigten eine negative Beziehung zwischen NF-κB p65 und PGC-1α Expression
In Kardiomyozyten, die IL-1α ausgesetzt sind, werden dieDie Achse NF-κB/PGC-1α wurde aktiviert
Über expression von PGC-1α oder Hemmung der NF-κB-Signal übertragungWieder hergestellte Mitochondrien funktion und umgekehrte Stoffwechsel defekte
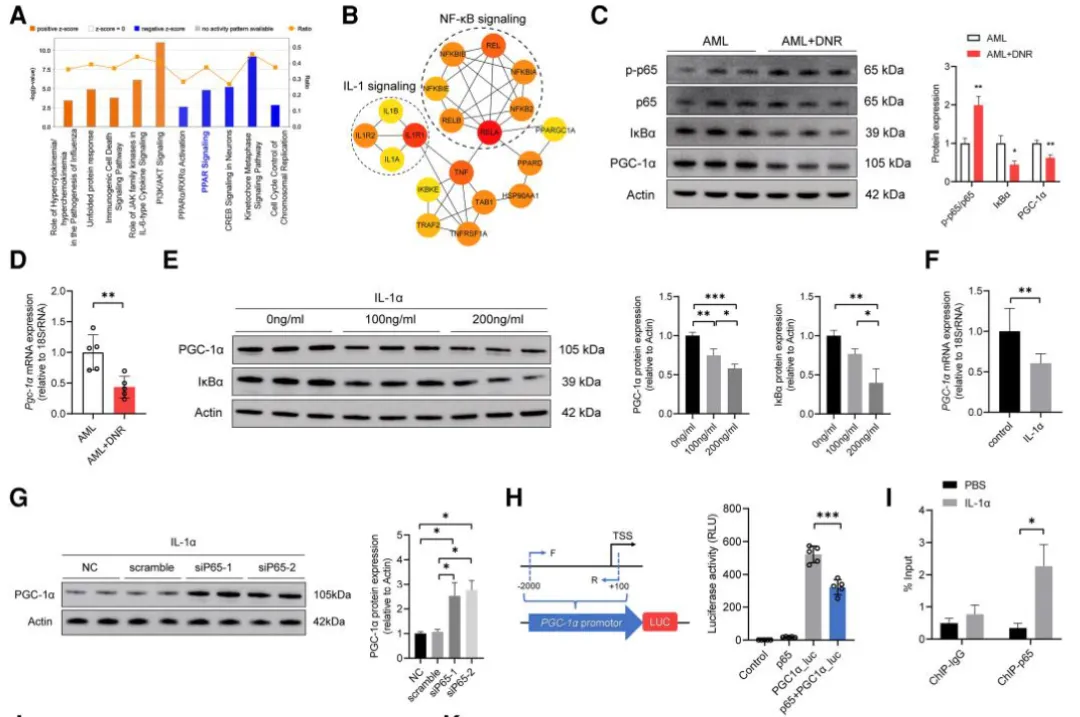
Abbildung 6. Die Achse IL-1α-NF-κB-PGC-1α reguliert den mitochondrialen Stoffwechsel des Herzens
Um das therapeut ische Potenzial der IL-1α-Blockade zu testen, wurden AML-DNR-Mäuse mit behandeltIL-1α-neutralisierende AntikörperOder IgG-Kontrollen:
Die Antikörper behandlung verbesserte die Herzfunktion deutlich
Myokard-ATP-Spiegel und mitochondriale Funktion wurden wieder hergestellt
Die Expression von PGC-1α-und Fettsäure stoffwechsel genen nahm zu
Die Unterdrückung von Leukämie blieb unberührt und bestätigte, dass die IL-1α-Blockade die Anti tumor wirksamkeit von DNR nicht beeint rächt igte
Diese Ergebnisse zeigen, dassDie Ausrichtung auf IL-1α kann eine wirksame Strategie seinZuChemo therapie induzierte Kardio toxizität mildernIn AML.
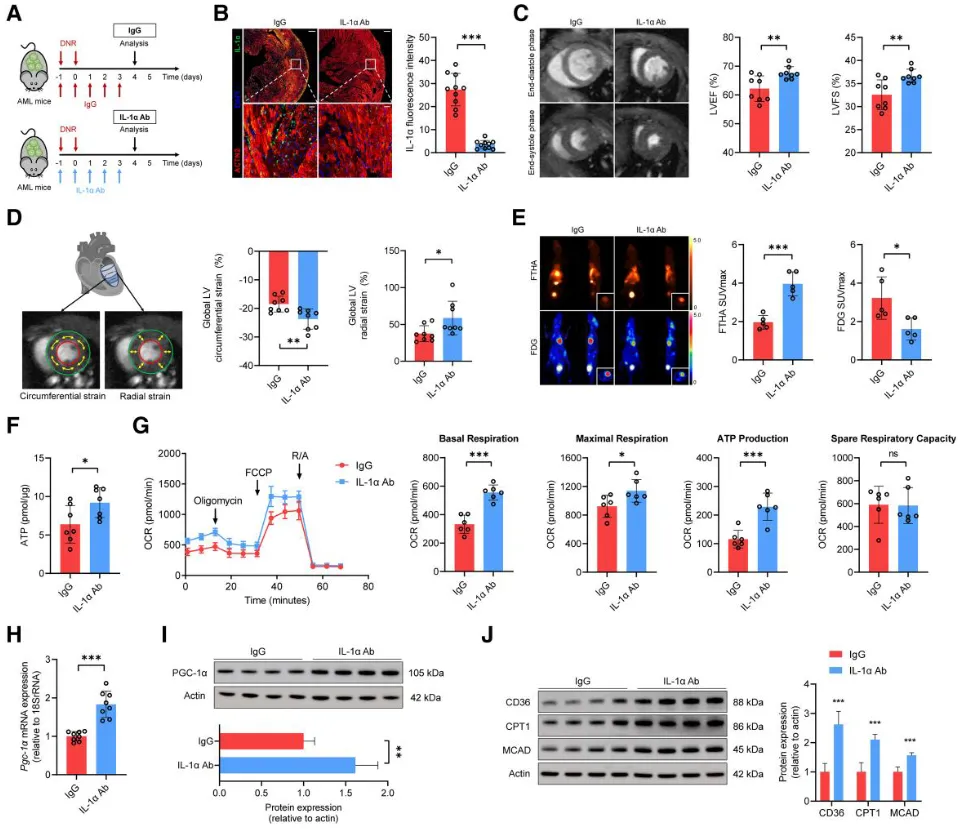
Abbildung 7. Die Behandlung mit Anti-IL-1α stellt die Herzfunktion wieder her, ohne die Wirksamkeit der Chemo therapie zu beeinträchtigen
Diese Studie kommt zu dem Schluss, dass während einer auf Daunorubicin (DNR) basierenden Chemo therapie bei AML-Patienten die Nekrose von Tumorzellen zur Freisetzung von IL-1α führt, einem proin flamm ato rischen Zytokin. IL-1α aktiviert die NF-κB-Signal übertragung im Herzen, was wiederum die Expression von PGC-1α-einem Schlüssel regulator des Herz energie stoffwechsels unterdrückt. Diese Unterdrückung stört die Fettsäure oxidation und reduziert die Energie erzeugung, was letztendlich die Herzfunktion beeint rächt igt.
Die Verab reich ung eines IL-1α-neutralisieren den Antikörpers in AML-Mausmodellen kehrte die durch Chemo therapie induzierten Stoffwechsel störungen erfolgreich um und stellte die Herzfunktion wieder her, ohne die antileukä mische Wirksamkeit von DNR zu beeinträchtigen.
Diese Ergebnisse legen nahe, dass die IL-1α-Blockade eine viel versprechende therapeut ische Strategie zur Verringerung der Kardio toxizität und zur Verbesserung der Langzeit ergebnisse für AML-Patienten darstellt, die sich einer Chemo therapie unterziehen.
In dieser Forschung war die Einzel kern-RNA-Sequenz ierung (snRNA-seq) entscheidend für die Erfassung der Transkript ions landschaft von menschlichen und Maus-Kardiomyozyten nach einer DNR-basierten Chemo therapie. Omics Empower unterstützte diese Phase durch zuverlässige BereitstellungSnRNA-seqDienstleistungen, die eine hoch auflösende Kartierung von Herz zell populationen und metabolischen Gen signaturen ermöglichen.
Unsere Einzel kern-und Einzel zell sequenz ierungs dienste sind für fragile klinische Proben wie Herz biopsien optimiert, und unser Bioinformatik-Team stellt eine robuste nach gelagerte Analyse sicher, die auf die Hypothese jeder Studie zuges chnitten ist.
Wir haben über 400 von Experten begutachtete Veröffentlichungen in Zeitschriften unterstützt, darunter Nature, Cell, Cancer Cell und European Heart Journal.Kontaktieren Sie unsUm heraus zu finden, wie unsere Single-Cell-Sequencing-und Multi-Omics-Services Ihre Forschung beschleunigen können.
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong