
Hülsen früchte hängen von symbiotischen Wechsel wirkungen mit Rhizobien ab, um ihren Stickstoff bedarf zu decken. Es bleibt jedoch unklar, wie diese Pflanzen eine nützliche Rhizobie tolerieren und gleichzeitig eine wirksame Immunität gegen Krankheits erreger aufrechterhalten.
Am 6. Mai 2025 ver öffentlichte die Gruppe von Prof. Ertao Wang an der Chinesischen Akademie der Wissenschaften eine Studie in Nature mit dem Titel"Ein Kinase mediator für rhizobiale Symbiose und Immunität in Medicago"Und enthüllt einen neuartigen Mechanismus, der diesem Gleichgewicht zugrunde liegt. Unter Verwendung einer von Omics Empower erstellten Medicago-Hefe-cDNA-Bibliothek ident ifi zierte das Team MtLICK1/2-ein Paar zytoplasma tischer Kinasen, die mit dem Nod-Faktor-Rezeptor MtLYK3 interagieren. Diese Kinasen koordinieren sowohl den Aufbau einer Symbiose als auch die Unterdrückung pflanzlicher Immunantworten.

Hefe bibliothek: Medicago truncatula cDNA-Expressions bibliothek (konstruiert vonOmics Empower)
Köder protein: MtLYK3 (zytoplasma tische Domäne)
Screening-Methode: Hefe-Zwei-Hybrid (GAL4-System)
Validierung: Y2H-Assay, Fluoreszenz-Co-Lokal isierung, Co-Immun präzipitation (Co-IP)
* Service Provider: Die in diesem Projekt verwendete Medicago-Hefe-cDNA-Bibliothek wurde von Omics Empower erstellt. Wenn Sie nach ähnlichen suchenHefe bibliothekLösungen-einschl ießlichBibliotheks bauUndScreening-Unser Team bietet End-to-End-Support, der auf Ihre Forschungs bedürfnisse zuges chnitten ist.
Durch Hefe-Zwei-Hybrid-Screening wurde MtLICK1 als starker Inter aktor von MtLYK3 ident ifi ziert. Die phy logen tische Analyse ergab, dass MtLICK1 zu einer konservierten RLK-Unterfamilie gehört, die in arbuskulären Mykorrhiza pflanzen vorkommt. Sein Homolog MtLICK2 interagiert auch spezifisch mit MtLYK3 und bildet einen Rezeptor komplex an der Plasma membran.
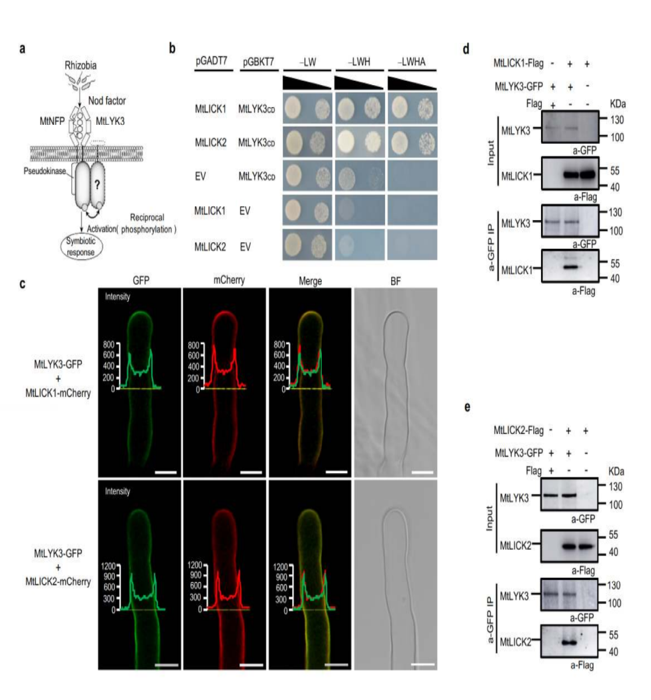
Abbildung 1. Wechsel wirkung zwischen MtLYK3 und MtLICK1/2
Um zu untersuchen, ob MtLICK1 und MtLICK2 an der rhizobialen Symbiose beteiligt sind, untersuchten die Forscher zunächst ihre Expressions niveaus. Beide Gene wurden nach Nod-Faktor-Behandlung oder Inokulation mit Sinorhizobium meliloti signifikant hoch reguliert. Promoter-GUS-Assays zeigten, dass pMtLICK1::GUS und pMtLICK2::GUS haupt sächlich in Wurzelhaaren und der Dehnung szone exprimiert wurden. Nach einer Rhizobial infektion lokalisierte sich ihre Expression auf Knollen primo rdia und die Infektions zone reifer Knötchen und zeigte ein ähnliches Muster wie pMtLYK3::GUS.
Um die Funktion weiter zu bewerten, generierte das Team Mtlick1-, Mtlick2-und Mtlick1/2-Mutanten. Bei der Impfung mit S. meliloti 1021 zeigten alle Mutanten eine signifikant verringerte Knoten bildung. Insbesondere konnten Mtlick1/2-Doppelmutanten keine funktionellen rosa Knötchen bilden und zeigten selbst nach 21 oder 28 Tagen nur wenige kleine Beulen, ohne dass eine Stickstoff fixierung nachweisbar war. Das Stumm schalten von MtLICK1 im Mtlick2-Hintergrund unter Verwendung von RNAi führte zu einer weiteren Abnahme der Knoten, während die genetische Komplement ierung den Phänotyp wieder herstellte. Zusammen genommen zeigen diese Ergebnisse, dass MtLICK1 und MtLICK2 redundant als Schlüssel regulatoren der Rhizobial infektion und der Knötchen entwicklung fungieren.
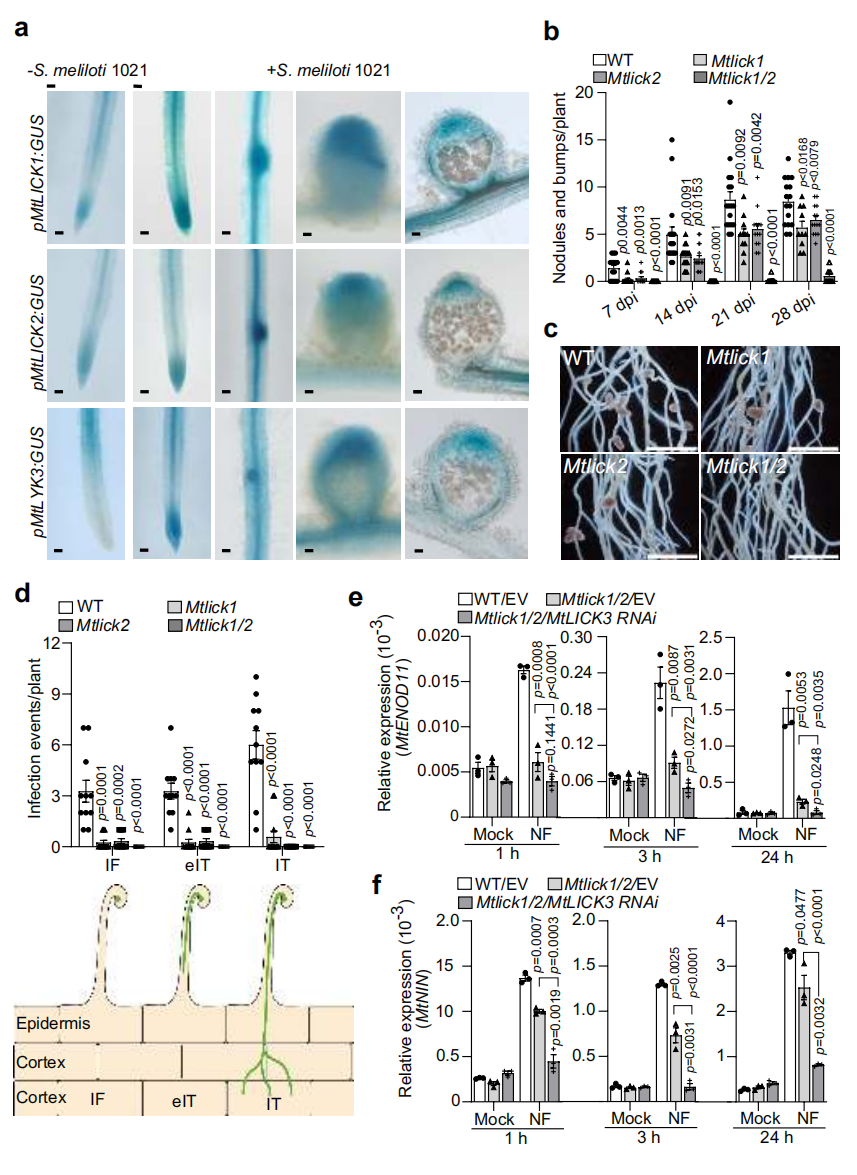
Abbildung 2. MtLICK1 und MtLICK2 sind essentiell für die rhizobiale Symbiose
Um zu testen, ob MtLICK1/2 als Signal kinasen im Nod-Faktor-Weg fungiert, haben die Autoren die Expressions niveaus symbiotischer Marker gene gemessen (MtMIN, MtENOD11). Im Vergleich zum Wildtyp zeigte die Mtlick1/2-Doppelmutante eine signifikant reduzierte Expression, was auf eine entscheidende Rolle für MtLICK1/2 bei der Initiierung der symbiotischen Signal übertragung hinweist.
In-vitro-Kinase-Assays bestätigten, dass beide Proteine eine Auto phosphor ylierung und eine Trans phosphor ylierungs aktivität aufweisen. Sequenz ausrichtung und orts gerichtete Mutagenese ident ifi zierten wichtige ATP-Bindungs residues-K78 in MtLICK1 und K73 inMtLICK2-as essentiell für ihre Kinase funktion (Abb. 3a).
Die Massen spektrometrie ident ifi zierte drei MtLYK3-mediated Phosphor ylierungs stellen in MtLICK1/2, die sich innerhalb der P-Schleife und der Aktivierung schleife ihrer Kinase domänen befinden. Phospho-mimische Mutanten (e.g., mtLICK1 ^ S60D ^, MtLICK2 ^ S55D ^, MtLICK1/2 ^ 3D ^) zeigte eine erhöhte Kinase aktivität und eine vollständig gerettete Knoten bildung in der Mtlick1/2-Mutante. Im Gegensatz dazu konnten nicht phosphor ylat ierbare Varianten (z. B. MtLICK1/2 ^ 3A ^) die Funktion nicht wiederherstellen (Abb. 3b-e).
Weitere Experimente zeigten, dass die Nod-Faktor-Wahrnehmung MtLYK3 aktiviert, das dann MtLICK1/2 phosphor yliert. Bei der Phosphor ylierung zeigt MtLICK1/2 eine verringerte Wechsel wirkung mit einem MtLYK3-suggesting Freisetzung mechanismus für die nach geschaltete Signal übertragung (Abb. 3f-g).
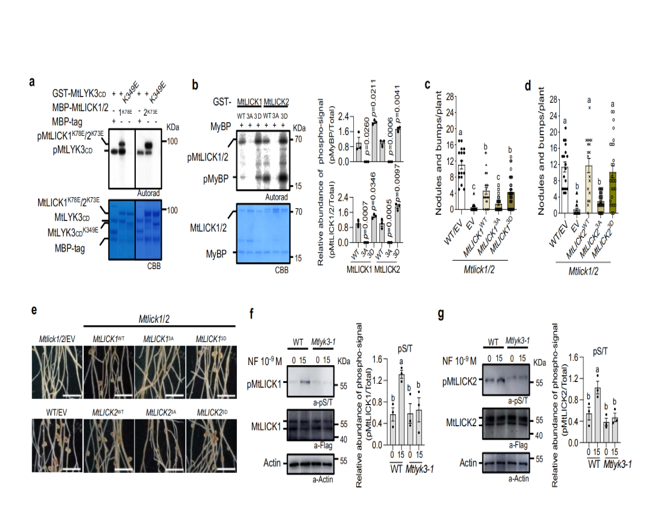
Abbildung 3. MtLYK3 phosphor yliert MtLICK1/2, um die rhizobiale Symbiose zu regulieren.
Aufgrund ihrer Trans phosphor ylierungs aktivität stellten die Autoren die Hypothese auf, dass MtLICK1/2 auch MtLYK3 aktivieren könnte. In-vitro-Kinase-Assays bestätigten dies: katalytisch inaktive MtLYK3 ^ K349E ^ konnte sich nicht selbst phosphor ylieren, sondern wurde durch rekombinantes MtLICK1 ^ WT ^ und MtLICK2 ^ WT ^ phosphor yliert (Abb. 4a). MtLICK1/2 verbesserte die MtLYK3-Phosphorylierung sowohl in In-vitro-als auch in-vivo-Assays signifikant (Abb. 4b).
Acht Phosphor ylierungs stellen auf MtLYK3 wurden ident ifi ziert, einschl ießlich T472, T475, T480 und Y483 innerhalb des Aktivierung segments. Die Alanin substitution an diesen Stellen beeint rächt igte die Nodulation. Insbesondere fehlte MtLYK3 ^ Y483F ^ die Kinase aktivität und konnte die Nodulation oder Gen expression in Mtlyk3-1 Mutanten nicht retten (Abb. 4c-d). Dieses mutierte Protein war ebenfalls instabil, was darauf hindeutet, dass Y483 zur MtLYK3-Stabilität beiträgt.
Eine weitere wichtige Stelle, Y488, liegt innerhalb des konservierten YAQ-Motivs, von dem bekannt ist, dass es das Gleichgewicht zwischen Symbiose und Immunität in Lotus vermittelt. Anti-phospho-Y488 Antikörper zeigten, dass die Nod-Faktor-induzierte Y488-Phosphorylierung von MtLICK1/2 abhängt (Abb. 4e-f). Die MtLYK3 ^ Y488F ^-Mutante konnte keine symbiotischen Marker aktivieren oder die Nodulation wiederherstellen (Abb. 4g-h), was die wesentliche Rolle von Y488 hervor hob. Ferner phosphor yliert MtLYK3 die nach geschaltete Kinase MtDMI2-but diese wurde in der Y488F-Mutante abgeschafft.
Nicht phosphor ylatable MtDMI2-Varianten konnten auch die Nodulation nicht wiederherstellen, was die Notwendigkeit dieser Phosphor ylierungs kaskade bestätigte.
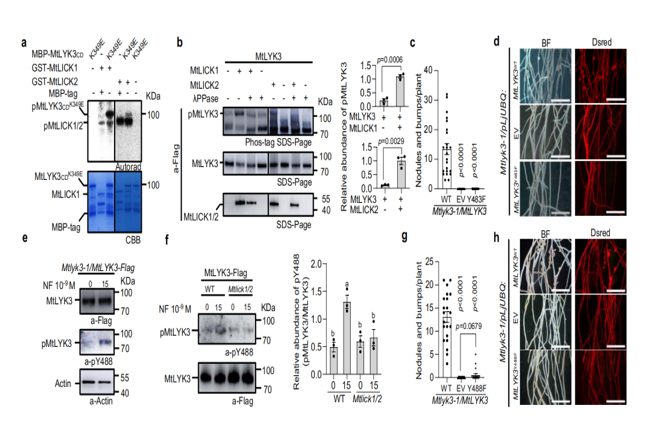
Abbildung 4. Die MtLICK1/2-vermittelte Phosphor ylierung von MtLYK3 ist für die Symbiose wesentlich.
Im Vergleich zum Wildtyp zeigten Mtlick1-, Mtlick2-und Mtlick1/2-Mutanten nach S. erhöhte Immunantworten. Meliloti-Impfung, einschl ießlich erhöhter MAPK-Aktivierung, ROS-Akkumulation und erhöhter Expression von Immun marker genen (Abb. 5a-d).
Um die breitere Immun funktion zu beurteilen, wurden Pflanzen mit dem Erreger Ralstonia solana cearum heraus gefordert. Wildtyp pflanzen waren anfälliger als die Mutanten, was darauf hindeutet, dass MtLICK1/2 normaler weise die Immunität unterdrückt, um die Besiedlung von Rhizobialen zu erleichtern.
Wenn Wildtyp pflanzen sowohl mit Nod-Faktoren als auch mit Ralstonia behandelt wurden, stieg die Anfälligkeit für Infektionen. Die Mtlick1/2-Mutanten zeigten jedoch keine solche Verstärkung, was darauf hinweist, dass die Nod-Faktor-vermittelte Immun suppression MtLICK1/2 erfordert (Abb. 5f).
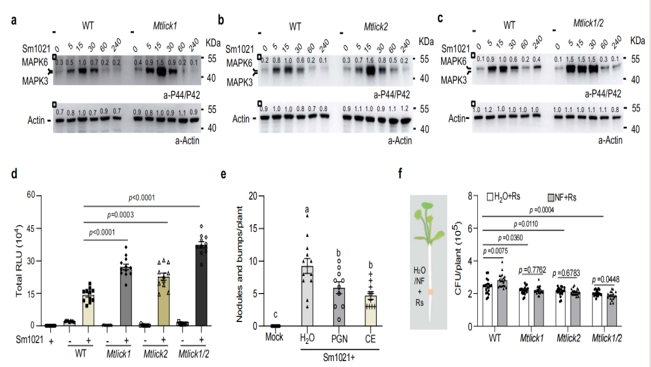
Abbildung 5. MtLICK1/2 schwächen Immunantworten ab, um die Symbiose zu fördern.
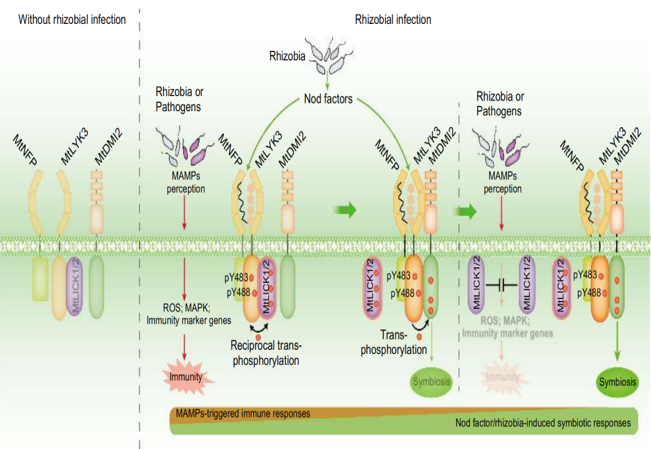
Abbildung 6. Doppelrollen von MtLICK1/2 bei der symbiotischen Signal übertragung und Immun regulation.
Diese Studie zeigt, dass MtLICK1 und MtLICK2 spezifisch mit dem Nod-Faktor-Rezeptor MtLYK3 interagieren und während der Etablierung einer rhizobialen Symbiose an der reziproken Phosphor ylierung teilnehmen. MtLICK1/2 initiiert nicht nur die symbiotische Signal übertragung, sondern optimiert auch die Immunantwort der Pflanzen, um die Kompatibilität mit Rhizobien sicher zustellen und gleichzeitig eine Über aktivierung der Verteidigung swege zu verhindern. Diese Ergebnisse liefern neue Erkenntnisse darüber, wie Hülsen früchte Symbiose und Immunität auf molekularer Ebene koordinieren.
Referenz
Wang, D., Jin, R., Shi, X. et al. Ein Kinase mediator für rhizobiale Symbiose und Immunität in Medicago. Natur (2025). https://doi.org/10.1038/s41586-025-09057-0
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong