
Am 28. März 2025,WissenschaftVer öffentlichte eine von Experten begutachtete Studie von Forschern der King Abdullah University of Science and Technology (KAUST), des australischen CSIRO und mehrerer kooperieren der Institutionen. Die Studie berichtet über einen molekularen Mechanismus, durch den Weizen Puccinia graminis f. sp. tritici, dem Erreger des Stamm rosts, widersteht. Die Ergebnisse identifizieren ein Zwei-Gen-System mit einer Tandem kinase und einem NLR-Protein, die koordiniert wirken, um pathogen spezifische Immunantworten auszulösen.
Diese Forschung trägt zum breiteren Verständnis der Pflanzen immunität bei und kann künftige Bemühungen zur Verbesserung der Krankheits resistenz in Weizen durch genetische Ansätze unterstützen.
* Dienst leister: EinigeHefe-Zwei-Hybrid-ScreeningDie Dienstleistungen wurden von Omics Empower erbracht. Wenn Sie nach ähnlichen suchenHefe bibliothekLösungen-einschl ießlichBibliotheks bauUndScreening-Unser Team bietet End-to-End-Support, der auf Ihre Forschungs bedürfnisse zuges chnitten ist.
Stamm rost bleibt eine der schädlich sten Pilz krankheiten, die die weltweite Weizen produktion beeinträchtigen. In einer früheren Studie klonierte das KAUST-Team ein Resistenz gen, Sr62TK, von Aegilops sharon ensis, einem wilden Weizen verwandten. Sr62TK codiert eine Tandem kinase, von der gezeigt wurde, dass sie bei Einführung in anfällige Weizen linien einen teilweisen Widerstand verleiht.
Weitere Untersuchungen ergaben jedoch, dass Sr62TK allein nicht ausreichte, um die Immunantwort vollständig zu aktivieren. Nachfolgende Analyse ident ifi zierte ein benachbartes Gen, das jetzt alsSr62NLRAls wahr schein licher Co-Faktor, der am Widerstands mechanismus beteiligt ist.
Genetische Kartierung und funktionelle Untersuchungen bestätigten, dassSr62NLRIst für Sr62TK-mediated Verteidigung erforderlich. Bei anfälligen Mutanten blieb die Sr62TK-Sequenz unverändert, aber Sr62NLR wurde mutiert und mit Widerstands verlust gemeinsam getrennt.
Komplement ierungs tests zeigten weiter, dass beideSr62TK und Sr62NLR müssen zusammen ausgedrückt werdenUm eine spezifische Immunantwort gegen den Pilz effektor auszulösenAvrSr62.
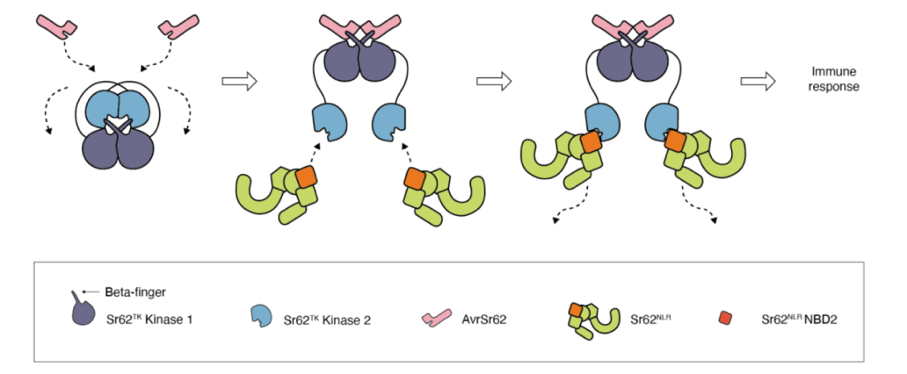
Die Forscher verwendeten strukturelle Modellierung und molekular biologische Techniken, um ein dreistufiges Aktivierung modell zu beschreiben:
1. effekt erkennung:Die Kinase1-Domäne von Sr62TK interagiert direkt mit AvrSr62, wie durch Hefe-Zwei-Hybrid-und Co-Immun präzipitation tests gezeigt.
2. Konformation änderung und Signal relais:Bei der Effektor bindung erfährt Sr62TK strukturelle Änderungen, die die Kinase2-Domäne freilegen, die dann mit Sr62NLR assoziiert wird.
3. Immun aktivierung:Diese Wechsel wirkung löst nach geschaltete Immunantworten aus. Die konservierte Grenzfläche zwischen Kinase2 und Sr62NLR deutet auf eine funktionelle Stabilität im Signal prozess hin.
Die Studie stellte auch fest, dassKinase1 ist relativ variabelDies ermöglicht möglicher weise die Anpassung an die Entwicklung von Krankheits erregern, währendKinase2 und Sr62NLR sind konservierterWahr schein lich die Signal zuverlässigkeit bewahren.
AlphaFold2 wurde verwendet, um die Struktur des Sr62TK-Sr62NLR komplexes vorher zusagen. Die Modelle schlugen vor:
Kinase1 bildet ein Homo dimer über eine β-Strang-Grenzfläche.
Kinase2 vermittelt die Interaktion mit Sr62NLR und unterstützt die Konformation flexibilität.
Die standort gerichtete Mutagenese gegen 21 Reste trug zur Validierung wichtiger struktureller Vorhersagen bei. Insbesondere durch die Störung der Kinase1-Dimer-Grenzfläche wurde die Protein interaktion abgeschafft, während Mutationen in AvrSr62 ihre Erkennung veränderten und die Rolle dieser Domänen bei der Immunsignal isierung bestätigten.
Lu P. et al. (2025). Ein Weizen-Tandem kinase-und NLR-Paar verleiht Resistenz gegen mehrere Pilz pathogene. Wissenschaft, 387, 1418-1424. DOI: 10.1126/wissenschaft. adp5469
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong