
Eine kürzlich von Dr. Jiulin Du durchgeführte Studie der Forschungs gruppe hat einen neuartigen Mechanismus entdeckt, der die neuronale Aktivität mit der Entwicklung des Lymphsystems des Gehirns verbindet-vermittelt durch eine bestimmte Population von Gliazellen. Die Arbeit, die am 30. April 2025 in Cell ver öffentlicht wurde, trägt den Titel "Neural aktivität regulierte und Glia-vermittelte Kontrolle der lymphatischen Entwicklung des Gehirns".
Mithilfe der Einzelzell-RNA-Sequenz ierung ident ifi zierte das Team eine Sub population von radialen astro zyten ähnlichen Glia, die durch die slc6a11b-Expression gekennzeichnet ist. Es wurde festgestellt, dass diese Zellen Vegfc absondern, einen Schlüssel faktor, der die Entwicklung von meningealen lymphatischen Endothel zellen (MuLECs) antreibt. Interessanter weise wird die Sekretion von Vegfc durch neuronale Aktivität moduliert, was auf ein zuvor nicht erkanntes Übersprechen zwischen Neuronen und dem sich entwickelnden Lymphsystem hindeutet.
Um diesen Mechanismus weiter zu analysieren, verwendete die Studie eine bedingte Gen editier ung und eine In-vivo-Kalzium bildgebung, was zeigt, dass die radialen Astro zyten nicht nur auf neuronale Hinweise reagieren, sondern die Bildung von Lymph gefäßen während der Gehirnent wicklung aktiv regulieren. Diese Entdeckung eröffnet neue therapeut ische Wege für neuro logische Störungen im Zusammenhang mit lymphatischer Dysfunktion.
* Dienst leister:Omics EmpowerZur Verfügung gestelltEinzelzellen-Transkriptom-Sequenz ierungs dienste. Wenn Sie nach ähnlichen suchenEinzelzelleOderRäumlichLösungen unterstützen in Ihrer eigenen Forschung,Unser ExperteWürde gerne helfen.
Das Nervensystem kann Immunantworten über definierte anatomische Wege sowohl unter physio logischen als auch unter patho logischen Bedingungen regulieren. Ob es auch eine Rolle bei der Gestaltung der Entwicklung des Immunsystems spielt-und wie-ist jedoch unklar geblieben.
Frühere Untersuchungen haben gezeigt, dass die Entwicklung von meningealen lymphatischen Endothel zellen (muLECs) von Vegfc-Vegfr3 Signal übertragung abhängt. MuLECs helfen dabei, Stoffwechsel abfälle aus dem Gehirn zu beseitigen, und sind für die Aufrechterhaltung der Immun-und Flüssigkeits homöostase unerlässlich. Daher ist die Identifizierung der zellulären Quelle von Vegfc und das Verständnis, ob die neuronale Aktivität die MuLEC-Entwicklung beeinflusst, der Schlüssel zur Verbesserung der therapeut ischen Strategien für lymphatische Dysfunktion des Gehirns.
Diese Studie zeigt, dass die neuronale Aktivität die Entwicklung von meningealen lymphatischen Endothel zellen (MuLECs) im Zebra fisch reguliert. Durch neuronale Modulation experimente zeigten die Forscher, dass Veränderungen der Gehirn aktivität die MuLEC-Bildung direkt beeinflussen.
Mithilfe der Einzelzell-RNA-Sequenz ierung ident ifi zierten sie slc6a11b-radiale Glia-ähnliche Zellen (RAs) als Hauptquelle für Vegfc, ein wichtiges Signal molekül, das die MuLEC-Entwicklung voran treibt. Das Team verwendete auch die bedingte Gen bearbeitung und die In-vivo-Calcium-Bildgebung, um die funktionelle Rolle von RAs zu untersuchen, und stellte fest, dass diese Zellen in direktem Kontakt mit MuLECs stehen.
Darüber hinaus bestätigte die Studie durch die Kombination von Calcium bildgebung, Augen entfernung und pharma ko logischen Hemmung experimenten, dass sowohl die RA-Aktivität als auch die Vegfc-Expression eng mit der neuronalen Aktivität verbunden sind. Diese Ergebnisse zeigen, dass neuronale Signale die MuLEC-Entwicklung regulieren, indem sie die Vegfc-Produktion in RAs steuern.
Um die Entwicklungs dynamik von meningealen lymphatischen Endothel zellen (MuLECs) zu untersuchen, erzeugten die Forscher transgene Zebra fisch linien. Sie beobachteten, dass MuLECs eine ring artige Struktur entlang der Grenze zwischen der Soma-und der Faser schicht des optischen Tektums (OT) bildeten.-eine Schlüssel region, die an der visuellen Verarbeitung beteiligt ist-und schrittweise erweitert, um die Oberfläche des OT zu bedecken (Abb. 1A-B).
Wenn die neuronale Aktivität unter Verwendung von Tricain pharma ko logisch unterdrückt wurde, wurde die Ring bildung blockiert und die Anzahl der MuLECs auf der OT-Oberfläche wurde signifikant reduziert (Abb. 1C-G).
Um die Rolle sensorischer Eingaben zu bewerten, entfernten die Forscher die Augen der Zebra fisch larven, um die visuelle Stimulation zu verringern. Dies führte auch zu einer deutlichen Verringerung der MuLEC-Zahlen auf der OT-Oberfläche (Abb. 1H-P).
Im Gegensatz dazu stieg die Anzahl der MuLECs in den stimulierten Larven signifikant an, wenn die elektrische Stimulation (ES) angewendet wurde, um die neuronale Aktivität zu erhöhen (Abb. 1Q-R).
Zusammen genommen liefern diese Ergebnisse starke Beweise dafür, dass die neuronale Aktivität eine regulator ische Rolle bei der Entwicklung von lymphatischen Strukturen des Gehirns spielt.
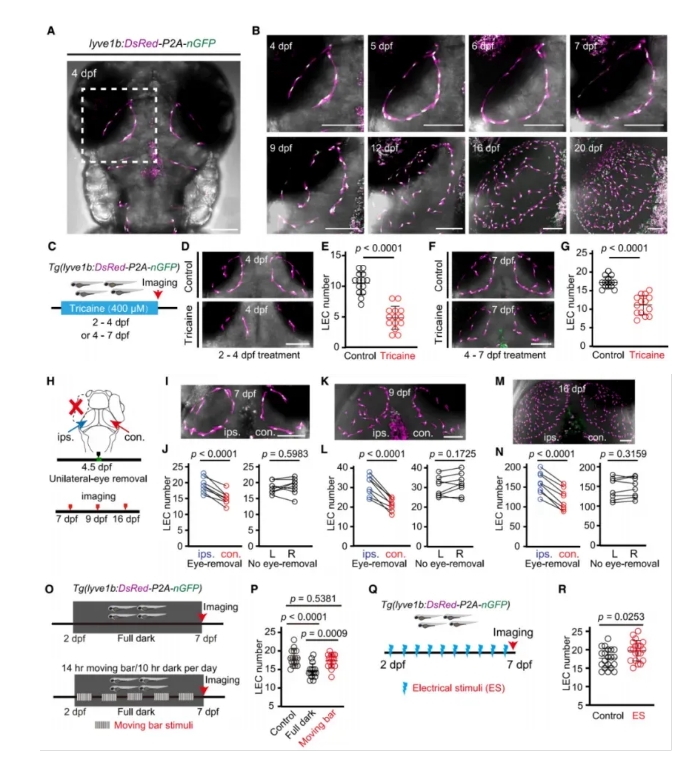
Abbildung 1. Neuronale Aktivität ReEntwicklung im Zebra fisch gulate muLEC
Vegfc und Vegfd sind sekret ierte Proteine, von denen bekannt ist, dass sie eine wesentliche Rolle bei der Entwicklung von Lymph gefäßen bei Wirbeltieren spielen. Um die Quelle dieser Faktoren im Gehirn zu identifizieren, führten die Autoren in drei Entwicklungs stadien eine Einzelzellen-RNA-Sequenz ierung an Ganzhirn proben von Zebra fischen durch.
Sie fanden heraus, dass radiale Glia-ähnliche Zellen (RAs) der vorherrschende Zelltyp waren, der sowohl Vegfc als auch Vegfd exprimierte (Abb. 2A-B).
Mithilfe einer KI-Reporter-Zebra fisch linie (Knock-In) visualisierten die Forscher Vegfcs RAs weiter, die haupt sächlich im gesamten Gehirn verteilt waren. Diese Zellen verlängerten die Prozesse in Richtung des Aderhaut-Gefäß plexus (CVP) und erreichten die Gehirn oberfläche, wo sie direkten Kontakt mit MuLECs hatten (Abb. 2C-E).
Die Subtyp analyze von RAs auf Einzelzellen ebene in Kombination mit der In-situ-Hybrid isierung bestätigte, dass slc6a11b-RAs die Hauptquelle für Vegfc und Vegfd im Gehirn waren. Diese Zellen zeigten die gleiche Morphologie wie die Vegfc-RAs und hielten direkten Kontakt mit MuLECs aufrecht (Abb. 2F-K).
Zusammen genommen zeigen diese Ergebnisse, dass slc6a11b-RAs die MuLEC-Entwicklung durch Vegfc-Signal übertragung regulieren.
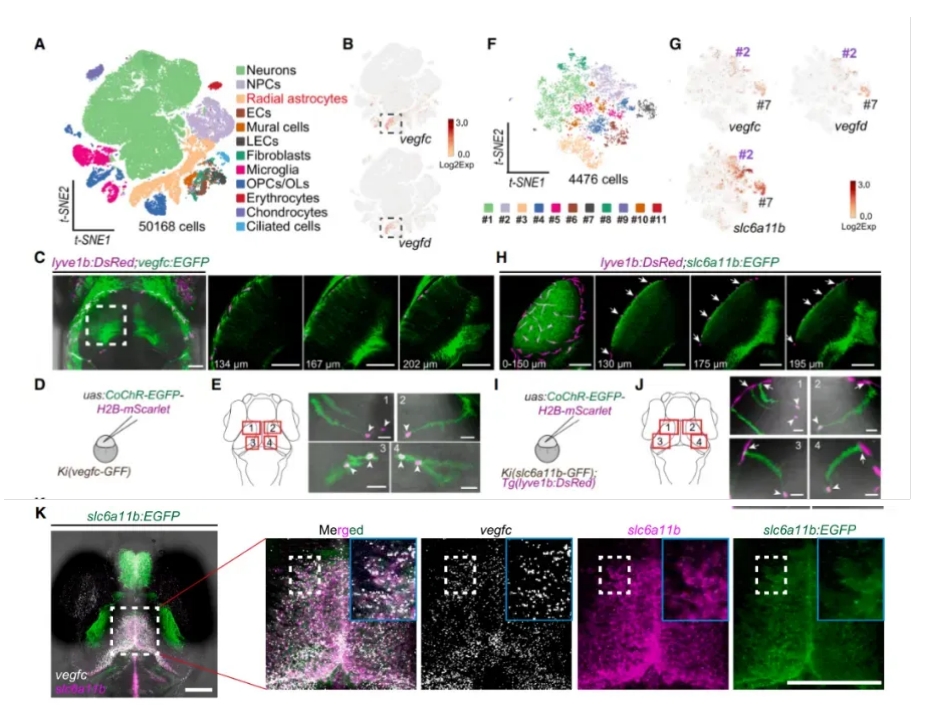
Abbildung 2. slc6a11b RAs sind die Hauptquelle für Vegfc/Vegfd im Gehirn
Um weiter zu untersuchen, ob slc6a11b-radiale glia ähnliche Zellen (RAs) die MuLEC-Entwicklung regulieren, führten die Autoren Experimente zum funktionellen Funktions verlust durch.
Sie behandelten Zebra fische mit Metro nidazol (MTZ), um slc6a11b RAs selektiv abzutragen. Dies führte zu einer beeint rächt igten MuLEC-Entwicklung, wie das Versagen der Ringstruktur bildung und eine signifikante Verringerung der MuLEC-Zahlen zeigt (Abb. 3A-C).
Als nächstes störte das Blockieren des Vegfc-Vegfr3 Signalwegs die MuLEC-Bildung. Umgekehrt verbesserte die Über expression von Vegfc speziell in slc6a11b-RAs die muLEC-Entwicklung (Abb. 3D-E).
Um die Spezifität des Zelltyps zu testen, führten die Forscher eine bedingte Vegfc-Knockout-und Über expression sowohl in slc6a11b-RAs als auch in pdgfras-Fibroblasten durch. Sie fanden heraus, dass nur die Manipulation in slc6a11b-RAs einen signifikanten Einfluss hatte, was bestätigt, dass diese Zellen eine dominierende Rolle bei der Regulierung der MuLEC-Entwicklung spielen (Abb. 3FJ).
Zusammen zeigen diese Ergebnisse, dass slc6a11b-RAs für die muLEC-Entwicklung über die Vegfc-Vegfr3 Signal isierungs achse wesentlich sind.
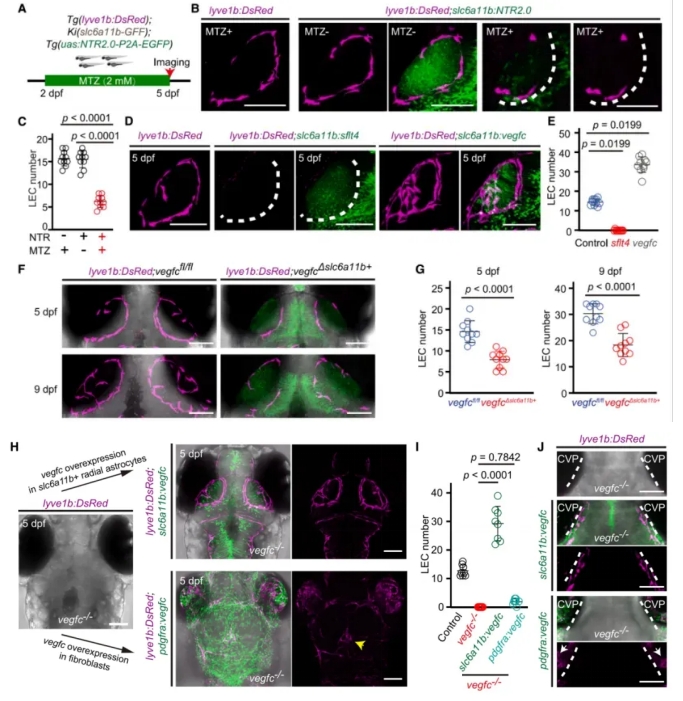
Abbildung 3. Der Ausdruck von Vegfc durch slc6a11b-RAs ist für die Entwicklung von muLEC von entscheidender Bedeutung
Um fest zustellen, ob slc6a11b-RAs und ihre Expression von Vegfc durch neuronale Aktivität reguliert werden, führten die Forscher eine Reihe von Experimenten zur funktionellen Bildgebung und Störung durch:
Unter Verwendung der zweifarbigen Kalzium bildgebung stellten sie fest, dass slc6a11b RAs auf Lichts timulation mit erhöhter Kalzium aktivität reagierten, ähnlich wie Neuronen im optischen Tektum (OT) neuro pil (Abb. 4A-D).
In einseitigen Augen entfernungs experimenten war die spontane Calcium aktivität in kontra lateralen OT-RAs im Vergleich zur ipsi lateralen Seite beeint rächt igt (Abb. 4E-H).
Die Vegfc-Expression in RA-Prozessen war auf der dem entfernten Auge entsprechenden Seite signifikant reduziert, obwohl die Anzahl der slc6a11b-RAs unverändert blieb (Abb. 4I-L).
Die Blockierung der neuronalen Aktivität pharma ko logisch führte auch zu einer verringerten Vegfc-Expression in diesen Zellen (Abb. 4M-Q).
Diese Ergebnisse zeigen, dass die neuronale Aktivität die Vegfc-Expression in slc6a11b-RAs positiv reguliert und dass eine reduzierte neuronale Eingabe zu einer Herunter regulierung von V führtEgfc, wodurch die muLEC-Entwicklung beeint rächt igt wird.
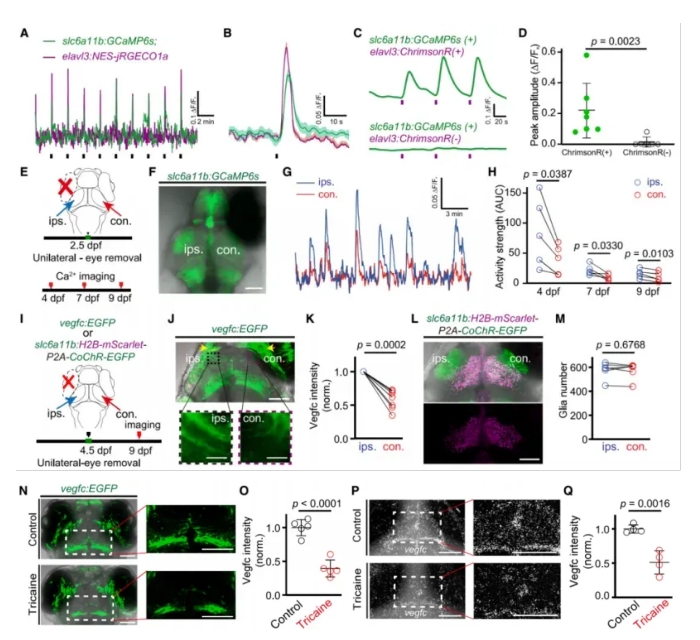
Abbildung 4. Aktivität und Vegfc-Ausdruck in slc6a11b-RAs sind an neuronale Signale gekoppelt
Als nächstes untersuchten die Forscher, ob die neuronale Aktivität die MuLEC-Entwicklung spezifisch durch die Vegfc-Expression in slc6a11b-RAs beeinflusst.
Sie führten Experimente zur Störung der neuronalen Aktivität-einschl ießlich einseitiger Augen entfernung und bewegter visueller Reize-in Zebra fischl arven mit bedingter Deletion von Vegfc in slc6a11b RAs (Vegfc c^ KO ^ slc6a11b) durch. Im Gegensatz zu Wildtyp-Kontrollen (Vegfc ^ fl/fl ^) hatten diese Manipulationen keinen Einfluss auf die MuLEC-Zahlen in den Vegfc-defizienten Larven (Abb. 5).
Die Über expression von Vegfc in slc6a11b-RAs rettete jedoch erfolgreich den Verlust von MuLECs, der durch visuellen Deprivat ion verursacht wurde.
Diese Ergebnisse zeigen, dass die neuronale Aktivität die MuLEC-Entwicklung über von Glia abgeleitetes Vegfc reguliert und dass slc6a11b-RAs als funktionelle Brücke zwischen neuronalen Signalen und lymphatischer Bildung fungieren.
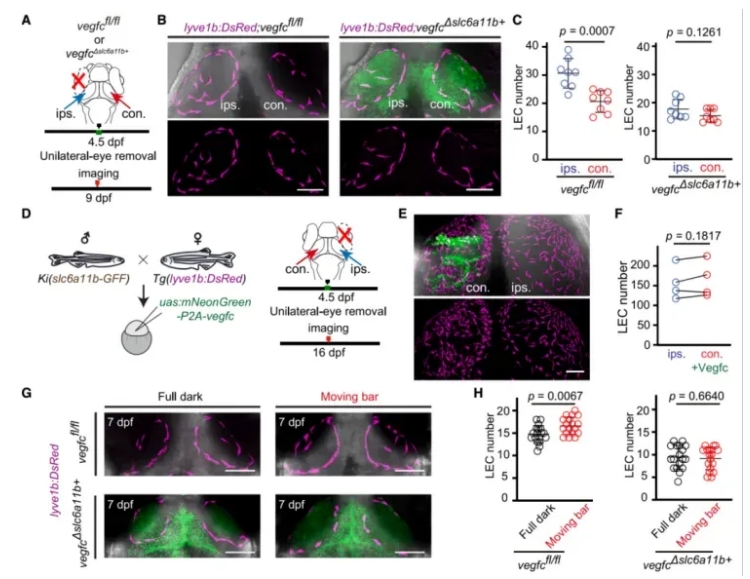
Abbildung 5. Neuronale Aktivität reguliert die muLEC-Entwicklung durch Vegfc-Expression in slc6a11b-RAs
Die vorherigen Ergebnisse zeigten, dass slc6a11b radiale Glia (RAs) die MuLEC-Entwicklung durch die Vegfc-Expression im Gehirn fördern. Während sich RAs tief im Gehirn parenchym befinden, sind MuLECs auf die meningeale Oberfläche beschränkt, was die Frage auf wirft: Was beschränkt MuLECs auf die Gehirn oberfläche, obwohl Vegfc intern produziert wird?
Um dies zu untersuchen, erzeugten die Forscher ccbe1-Knockout-Zebrafische und stellten fest, dass eine Über expression von Vegfc in slc6a11b-RAs die durch ccbe1-Verlust verursachten Entwicklungs defekte in MuLECs nicht retten konnte (Abb. 6A-C).
Mithilfe einer Klopf-in-Zebra fisch linie entdeckten sie, dass ccbe1 in Fibroblasten exprimiert wird, die an der Gehirn oberfläche lokalisiert sind (Abb. 6D). Wenn die reife Form von Vegfc in slc6a11b RAs ektopisch exprimiert wurde, wuchsen außerdem lymphatische Endothel zellen (LECs) im Gehirn parenchym und bildeten ektopische, lumen isierte Gefäße (Abb. 6E-G).
Diese Ergebnisse legen nahe, dass die räumliche Präzision der MuLEC-Bildung durch zwei räumlich unterschied liche Zell populationen gesteuert wird:
Slc6a11b-RAs im Gehirn parenchym, die Vegfc erzeugen
Ccbe1 ⁺ Fibroblasten an der Gehirn oberfläche, die die Reifung von Vegfc ermöglichen und seinen Funktions bereich einschränken
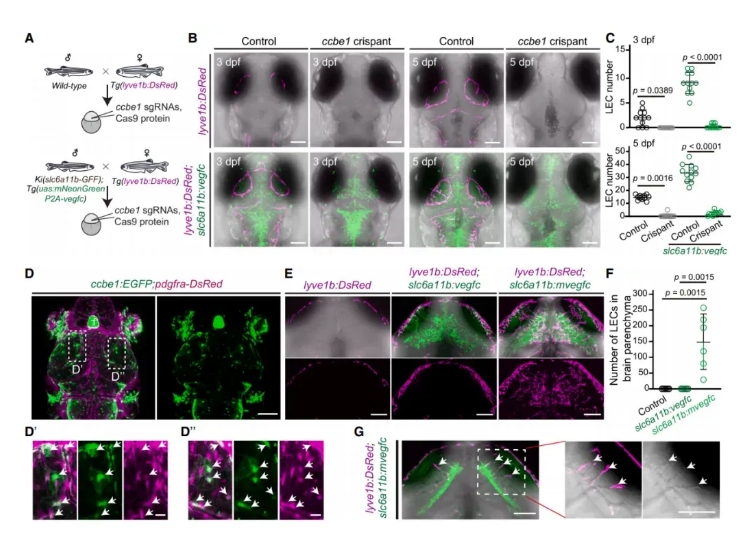
Abbildung 6. ccbe1, Fibroblasten und slc6a11b, RAs regulieren das muLEC-Muster kooperativ
Slc6a11b, radiale Glia (RAs) transportieren pro-Vegfc vom Gehirn zur meningealen Oberfläche. Dort kooperieren ccbe1-Fibroblasten mit RAs, um Pro-Vegfc in seine reife, aktive Form an der Grenzfläche zwischen dem Gehirn parenchym und den meningealen Fibroblasten umzuwandeln.
Dieser zweistufige, räumlich koordinierte Mechanismus stellt sicher, dass die Vegfc-Aktivität-und damit die MuLEC-Bildung-auf die Gehirn oberfläche beschränkt ist und die ektopische lymphatische Entwicklung im Gehirn verhindert.
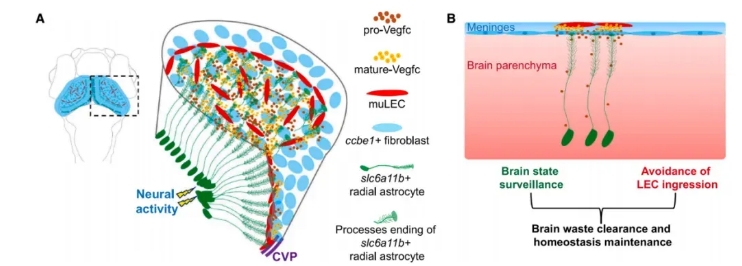
Abbildung 7. Arbeits modell der gehirn gesteuerten muLEC-Entwicklung
1. slc6a11b Die radiale Glia (RAs) sind die Hauptquelle für Vegfc im Gehirn.
2. Vegfc, hergestellt von slc6a11b, ist für die Entwicklung von muLEC unerlässlich.
3. Die neuronale Aktivität reguliert die MuLEC-Entwicklung durch Modulation der Vegfc-Expression in slc6a11b-RAs.
4. slc6a11b-RAs und ccbe1-Fibroblasten arbeiten zusammen, um die MuLEC-Bildung auf die Gehirn oberfläche zu beschränken.
Li J., Liu MJ, Du WJ, Peng XL, Deng H., Zi HX, Shang HB, Du JL. Neuronale Aktivität regulierte und Glia-vermittelte Kontrolle der lymphatischen Entwicklung des Gehirns. Zelle. 2025 Apr 22:S0092-8674(25)00410-6. doi: 10.1016/j.cell.2025.04.008.
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong