Magen-Adeno karzinom (GA)Ist eine der häufigsten und tödlichsten Krebsarten weltweit. Trotz ihrer Prävalenz bleibt die Krankheit schlecht verstanden-haupt sächlich aufgrund ihrer unklaren zellulären Herkunft und ihres hohen Grades an Tumor hetero genität. Wegen ihrer langen Lebensdauer,Magens tamm zellenAkkumulieren eher krebs treibende Mutationen, die zu einer malignen Transformation führen können.
Im Magen antrum,LGR5-basale StammzellenSind bekannte Marker von epithel ialen Stammzellen. Eine weitere wichtige Bevölkerung,4 StammzellenGekennzeichnet durchCCKBR (Cholecystokinin B-Rezeptor)Spielt eine Schlüssel rolle bei der Aufrechterhaltung des Stammzellen gleichgewichts und reagiert auf die Gastrin-Signal übertragung. Die Rolle vonCCKBRs Krebszellen-Insbesondere ihre Hetero genität und Relevanz für die Patienten ergebnisse-wurde nicht gut charakter isiert.
Eine von Prof. Hong Zheng von der Anhui Medical University durchgeführte Studie, ver öffentlicht in Cell Death & Differenzierung, zeigt eine entscheidende Rolle für CCKBRs stamm ähnliche Tumorzellen beim Fortschreiten des Magen adeno karzinoms.
Titel"CCKBRs Krebszellen tragen zur Intratumor-Hetero genität von Magenkrebs bei und verleihen Empfindlichkeit gegenüber FOXO-Hemmung."Das Papier verwendet die Einzelzell-RNA-Sequenz ierung (scRNA-seq), um eine eindeutige CCKBRs-Sub population mit stamm zell ähnlichen Merkmalen, einem einzigartigen Mutation profil und starken Verbindungen zu einer schlechten Patienten prognose zu identifizieren.
Wichtig ist, dass die Studie zeigt, dass die FOXO-Signal übertragung für die Aufrechterhaltung des Stammens und des Überlebens von CCKBRs Magenkrebs zellen unerlässlich ist und eine viel versprechende Richtung für gezielte Therapien bei Magenkrebs bietet.
* Omics EmpowerZur Verfügung gestelltEinzelzellen-Transkript om sequenz ierungs dienste.Wenn Sie nach ähnlichen suchenEinzelzelleOderRäumlichLösungen unterstützen in Ihrer eigenen Forschung,Unser ExperteWürde gerne helfen.
In dieser Studie verwendeten die AutorenEinzelzell-RNA-Sequenz ierung (scRNA-seq)Um eine Population von zu identifizierenCCKBRs stamm artige TumorzellenVerbunden mit schlechter Differenzierung und ungünstiger Prognose beim Magen adeno karzinom (GA). Es wurde gezeigt, dass diese Zellen einen signifikanten Beitrag zumIntra tumor ale Hetero genitätIn GA beobachtet.
Um ihre Ergebnisse zu validieren, führte das Team gezielte Analysen mit beiden eigenen scRNA-seq-Datensätzen durch(GSE183904)Und öffentlich zugängliche Daten vonDer Krebs genom atlas (TCGA).
Tabelle 1 fasst die klinischen Eigenschaften der über scRNA-seq analysierten Proben zusammen.
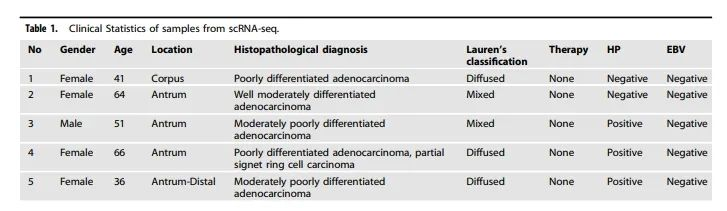
Das Team führte eine Einzelzell-RNA-Sequenz ierung (scRNA-seq) an Tumor proben von fünf Patienten mit Magen adeno karzinom (GA), vier Fällen von Magen antrum und einem Fall von Corpus krebs durch. Nach Qualitäts kontrolle und Ausreißer entfernung erhielten sie insgesamt 24.931 Zellen, die in acht Haupt zelltypen eingeteilt wurden. Sie konzentrierten sich auf Epithel zell cluster und ident ifi zierten 9 verschiedene Tumor epithel sub populationen über die t-SNE-Clustering von 6.568 Tumore pithel zellen. Alle Cluster zeigten hohe Malignität werte.
Ein Cluster particular-Epi5-was durch eine hohe CCKBR-Expression gekennzeichnet und markiert ihn als 4 stamm artige Zell population aus dem Magen antrum. Epi5-Zellen fehlten Differenzierung marker und sie exprimierten stattdessen stamm assoziierte Gene wie CD44, PROM1 und ALCAM, was auf eine starke Krebs stamm zelle hinweist (CSC) Potenzial.
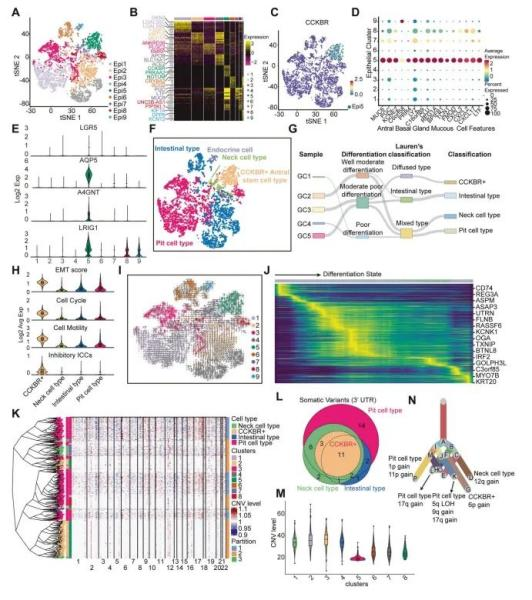
Abbildung 1. Die Einzeller-RNA-Sequenz ierung (scRNA-seq) ident ifi ziert CCKBRs stamm ähnliche Tumorzellen im Magen adeno karzinom (GA)
Um die Tumor hetero genität weiter zu untersuchen, wurden Epithel zellen in den intestinalen Typ, den foveolaren Typ, den Hals zelltyp, den CCKBRs-stamm artigen Typ und kleinere endokrine Subtypen eingeteilt. Unter ihnen wurden Epi5-Zellen als der primitivste und am schlechtesten differenz ierte Subtyp ident ifi ziert, der ein hohes Maß an Aggressivität assoziierten Genen wie CD74, REG3A und ASPM exprimiert.
Um fest zustellen, ob CCKBRs-Zellen aus 4 Stammzellen oder aus der Dedifferenzierung anderer Krebsarten stammen, analysierten die Forscher Schwankungen der Kopienzahl (CNVs) und der Evolutions linie in der Probe GC5. CCKBRs-Zellen zeigten eine ausgeprägte subklonale CNV-Struktur und die niedrigste CNV-Belastung, was die Ansicht stützt, dass sie eine separate Linie darstellen-kein dedifferenz iertes Produkt anderer Zelltypen.
Die Autoren führten eine immun histo chemische Färbung durch154 Magen gewebeprobenAus dem Antrum und dem Corpus zur Beurteilung der CCKBR-Expression über verschiedene Ebenen der Tumor differenzierung. In normalem Magen gewebe,CCKBR wird haupt sächlich in der Basal schicht der Antrum drüsen exprimiert,Und seine Expression nimmt mit der zellulären Differenzierung zunehmend ab. Im Gegensatz dazu,CCKBRs-Tumorzellen im Früh stadium zeigen eine starke Expression in den unteren Regionen der Magen drüsen, Wobei sich der Ausdruck im Verlauf des Tumors ausdehnt und ausbreitet(Abbildung 2A).
CCKBRs-Tumorzellen wurden auch in Lymphknoten metastasen ident ifi ziert, was auf das met astat ische Potenzial dieser Population hinweist. Darüber hinaus waren die CCKBR-Expressions niveaus bei CCKBRs-Tumoren im Vergleich zu benachbarten Nicht-Tumor geweben signifikant höher (Abbildung 2B).
Im Vergleich zu den fünf hoch regulierten Genen in GA zeigte CCKBR eine überlegene prädiktive Empfindlichkeit, was darauf hindeutet, dass es als potenzieller Biomarker für die Prognose von Magenkrebs nützlich ist. CCKBRs-Tumoren waren haupt sächlich antralen Ursprungs und zeigten eine starke Assoziation mit schlechter Differenzierung (Abbildung 2C). Diese Tumoren korrelierten auch mit einem geringeren Gesamt überleben und schlechteren Ergebnissen nach der Behandlung, wahr schein lich aufgrund einer höheren Wahrscheinlichkeit einer verbleibenden mikroskop ischen Tumor präsenz (ergänzende Abbildung 2C).
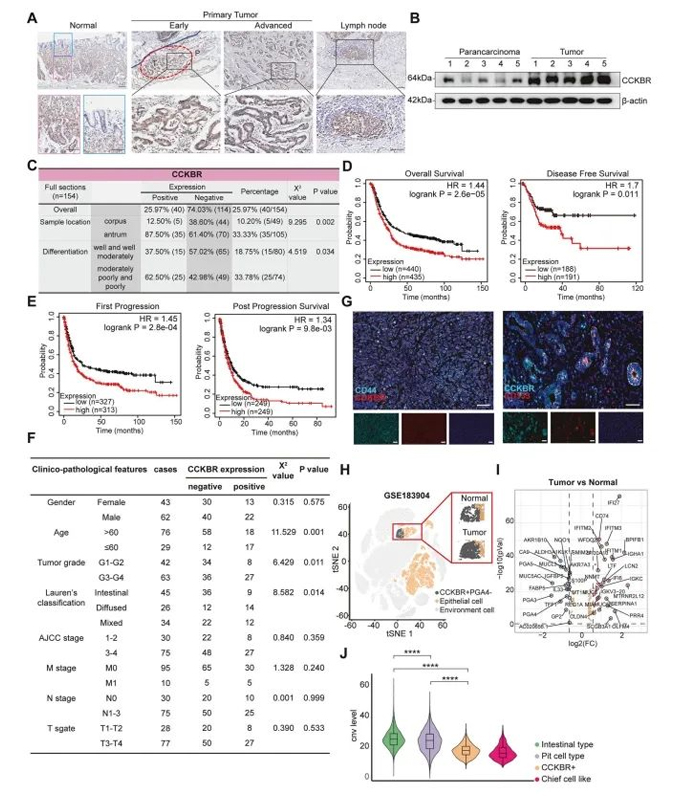
Abbildung 2. Die CCKBR-Expression ist mit einer schlechten Differenzierung und einer ungünstigen Prognose beim Magen adeno karzinom verbunden
Zusätzlich zur Expressions profilierung führten die Autoren klinisch-patho logische Analysen durch, in denen CCKBR-positive und CCKBR-negative Magen-Antrum tumoren verglichen wurden. CCKBR Tumoren waren signifikant assoziiert mit:
Jüngeres Patienten alter bei Diagnose (nachts ² = 11.529, p = 0,001)
Höherer Tumor grad (nachts ² = 6,429, p = 0,011)
Und der Lauren diffuse Subtyp (nachts ² = 8,582, p = 0,014)
Es wurde jedoch kein signifikanter Zusammenhang zwischen dem CCKBR-Status und der TNM-Inszenierung beobachtet (Abbildung 2F).
Die Studie berichtete auch über eine hohe Koexpression von CCKBR mit den Krebs stamm zell markern CD44 und CD133 (Abbildung 2G). unterstützt weiter die stamm artige Identität dieser Zellen, wie sie durch scRNA-seq offenbart wird.
Um eine Proben verzerrung aus zuschließen, validierten die Autoren ihre Ergebnisse unter Verwendung eines unabhängigen Einzelzellen-RNA-Seq-Datensatzes (GSE183904), der 40 Magenkrebs-und normale Gewebeproben umfasste. Die Analyse bestätigte, dass CCKBRs-Antral tumoren ein geringeres Differenzierung niveau und ein höheres malignes Potenzial aufweisen und mit einem signifikant schlechteren Überleben der Patienten verbunden sind.
Um genomische Veränderungen im Zusammenhang mit CCKBRs-Magen tumoren zu untersuchen, haben die Autoren Tumor proben aus dem Krebs genom atlas (TCGA) basierend auf der CCKBR-und Epi5-Marker-Expression geschichtet. Diese Tumoren zeigten ein DistiNct-Transkript ions profil, konsistent mit den Ergebnissen der Einzelzell-RNA-seq-Analyse.
Interessanter weise zeigten CCKBRs-Tumoren im Vergleich zu anderen Subtypen signifikant niedrigere Werte für die Tumor mutation belastung (TMB) und die Instabilität von Mikros atel liten (MSI). Die durchschnitt liche Mutation szahl pro Tumor wurde deutlich reduziert (193 gegenüber 0,602). Nach TCGA-Klassifizierung:
Die Inzidenz des MSI-Subtyps war bei CCKBRs-Tumoren reduziert (10,47% gegenüber 30,94%).
EBV-assoziierte Tumoren fehlten (0% gegenüber 10,07%)
Im Gegensatz dazu waren genom isch stabile (GS) Tumoren häufiger (16,28% gegenüber 8,63%)
Vor allem war der Anteil des Subtyps der chromosomalen Instabilität (CIN) wesentlich höher (72,09% gegenüber 48,92%).
L (Abbildung 3C)
Ein ähnlicher Trend wurde beobachtet, wenn Tumore unter Verwendung kanonischer Stamm zell marker, einschl ießlich LGR5, AQP5, A4GNT und LRIG1, neu klass ifi ziert wurden. Bestätigung, dass stamm ähnliche Tumorzellen eher zu GS-und CIN-Subtypen als zu MSI-oder EBV-Typen führen (Abbildung 3D).
Weitere genomische Profile ergaben, dass CCKBRs-Tumoren häufig durch Mutationen in TP53-, GLI3-, APC-und SMAD4-mutational mustern angetrieben werden, die mit der Entwicklung von CIN-und GS-Subtypen übereinstimmen (Abbildung 3H, 3J).
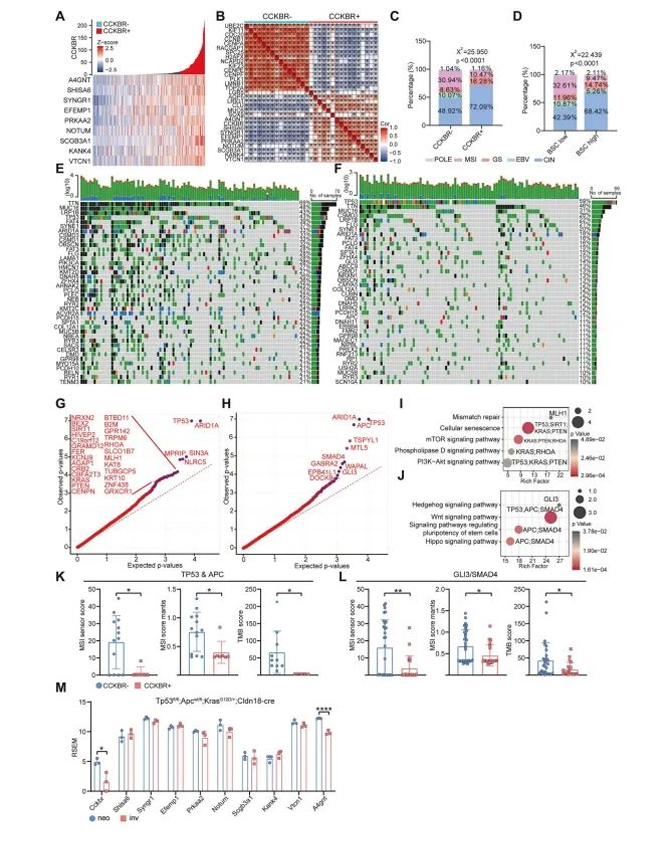
Abbildung 3. CCKBRs-Tumoren sind mit Chromosomen instabilität (CIN) und genom isch stabilen (GS) Subtypen angereichert
Um fest zustellen, ob TP53-, APC-, GLI3-und SMAD4-Mutationen direkt zur Bildung von CCKBRs-Tumoren beitragen, analysierten die Autoren Genom daten von CCKBR-positiven und CCKBR-negativen Patienten proben, die diese Mutationen tragen. Sie verglichen CNV-Profile (Copy Nummery Variation) über Gruppen hinweg.
Trotz des Vorhanden seins ähnlicher Treiber mutationen wiesen CCKBRs-Tumoren durchweg niedrigere TMB-und MSI-Werte auf als ihre CCKBRs-Gegenstücke (Abbildung 3K, 3L). was darauf hindeutet, dass diese Mutationen allein nicht ausreichen, um den CCKBRs-Tumor phänotyp zu erklären.
Um dies weiter zu validieren, untersuchten die Autoren ein Mausmodell des durch TP53-, APC-und KRAS-Mutationen induzierten Magen adeno karzinoms. Insbesondere wurden CCKBR-und Epi5-associated-Marker in diesen Modellen nicht hoch reguliert (Abbildung 3M).
Zusammen genommen deuten die Ergebnisse darauf hin, dass klassische Treiber mutationen zwar notwendig sind, aber nicht ausreichen, um den stamm artigen CCKBRs-Tumor phänotyp zu induzieren. Stattdessen muss eine maligne Transformation speziell in Magens tamm zellen erfolgen, da dieselben genetischen Veränderungen in Nicht-Stamm zell kontexten nicht zu dedifferenz ierten CCKBRs-Tumoren führen.
Um die biologischen Eigenschaften von CCKBRs-Tumorzellen zu untersuchen, führten die Autoren eine funktionelle Anreicherung analyze am Epi5-Cluster durch-der als stamm artig ident ifi zierten Sub population.
Epi5-Zellen waren haupt sächlich mit Pfaden assoziiert, die an Transkript ions initiation, Autophagie, Zell adhäsion, hypoxi scher Reaktion und Immun regulation beteiligt waren (Abbildung 4A und ergänzende Abbildungen 4A, 4B). Diese Signaturen legen nahe, dass CCKBRs-Zellen in einer hypox ischen Tumor mikro umgebung existieren und auf Autophagie und Adhäsion mechanismen für das Überleben und die Prolife ration beruhen.
Insbesondere zeigten Epi5-Zellen keine starke proliferative Signal übertragung, sondern wurden durch Transkript ions faktoren reguliert, die mit Entzündungen zusammenhängen (e.g., NFKB1, RELA, STAT3, ZFP36) und Stamm (e.g., JUN, FOXO3, FOXO4, CTNNB1) (Abbildung 4B).
Die Analyse der Pfad anreicherung ergab ferner die Aktivierung mehrerer Signal kaskaden, darunter:
NF-κB, TNF und IL-17 wege (entzündlich)
FOXO-, Nilpferd-, HIF-1-und TGF-β-Wege (Stammzellen-assoziiert)
Wichtig ist, dass der FOXO-Signalweg in Epi5-Zellen deutlich angereichert war (Abbildung 4C), was seine potenzielle Rolle bei der Aufrechterhaltung stamm ähnlicher Merkmale in CCKs BRMagenkrebs zellen unter streicht.
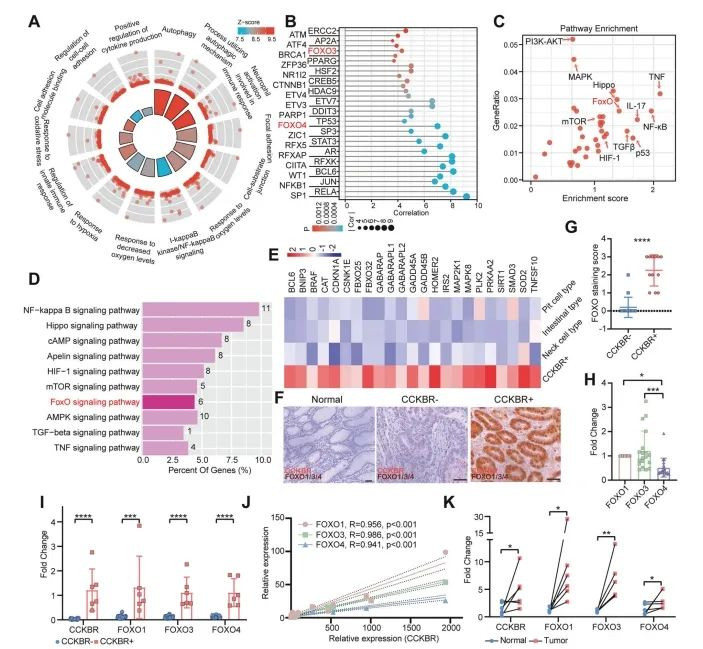
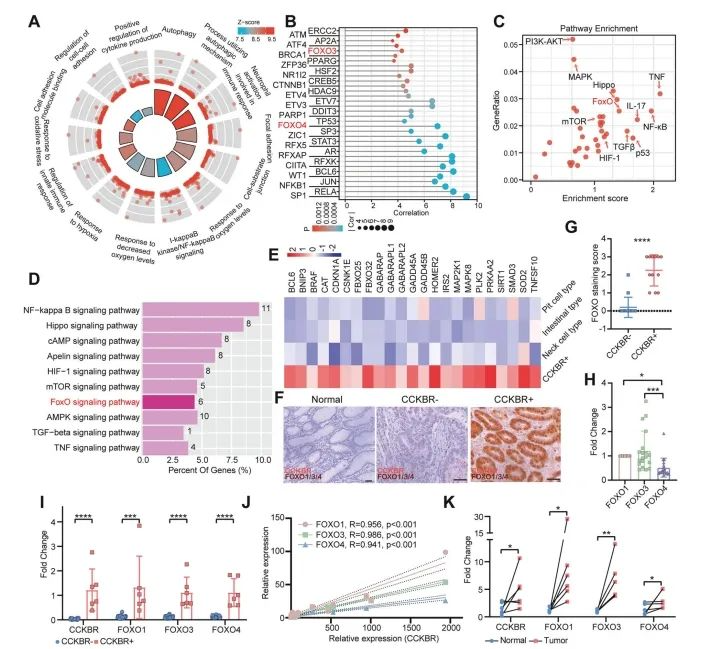
Abbildung 4. Verbesserte Aktivierung des FOXO-Signalwegs bei CCKBRs-Tumoren
Um die Anreicherung des FOXO-Signalwegs in einem unabhängigen Datensatz zu validieren, analysierten die Autoren GSE183094, das einen breiteren Satz von Magenkrebs und normalen Proben umfasst. Sie ident ifi zierten speziell eine Sub population von CCKBRs PGA4-Tumorzellen mit angereicherten FOXO-Signalweg-Signaturen (Abbildung 4D).
Sowohl in Epi5-Zellen als auch in CCKBRs-Tumorzellen von GSE183094 wurden Gene, die an der FOXO-Signal übertragung beteiligt sind, konstant hoch reguliert. Unterstützung der Feststellung, dass die FOXO-Aktivität ein Kennzeichen des Stamm-ähnlichen Tumor phänotyps CCKBRs ist (Abbildung 4E).
Um die funktionelle Relevanz der FOXO-Signal übertragung in CCKBRs-Tumorzellen zu bewerten, verglichen die Autoren CCKBR-positive und negative Zell populationen in Tests zur Bildung von Tumorsphären. Die Ergebnisse zeigten, dass CCKBR-Zellen eine deutlich größere Kapazität für die Erzeugung von Tumorsphären auf wiesen, was auf ein höheres Stamm potential hinweist (Abbildung 5B, 5C).
Um ihren Gehalt an Krebs stamm zellen (CSC) weiter zu bewerten, wurde ein begrenzter Verdünnung transplantation stest unter Verwendung von HGC27-Magenkrebszellen durchgeführt, die für die CCKBR-Expression sortiert und in immun defiziente Mäuse injiziert wurden. CCKBRs-Zellen bildeten im Vergleich zu ihren CCKBR-Gegenstücken signifikant größere Tumoren (Abbildung 5D-G und ergänzende Abbildung 5B).
In vitro führte die Tumorsphäre kultur zu einer erheblichen Hoch regulation von CCKBR-und FOXO1/3/4-Proteinen über sechs verschiedene Magenkrebs zelllinien im Vergleich zur Standard kultur (Abbildung 5H, 5I). Zusätzlich war die Expression von FOXO1, FOXO3 und FOXO4 in Tumorsc halen konstant erhöht (Abbildung 5J, 5K), was ihre Rolle bei der Aufrechterhaltung der CSC-ähnlichen Eigenschaften in CCKBRs-Zellen weiter unterstützte.
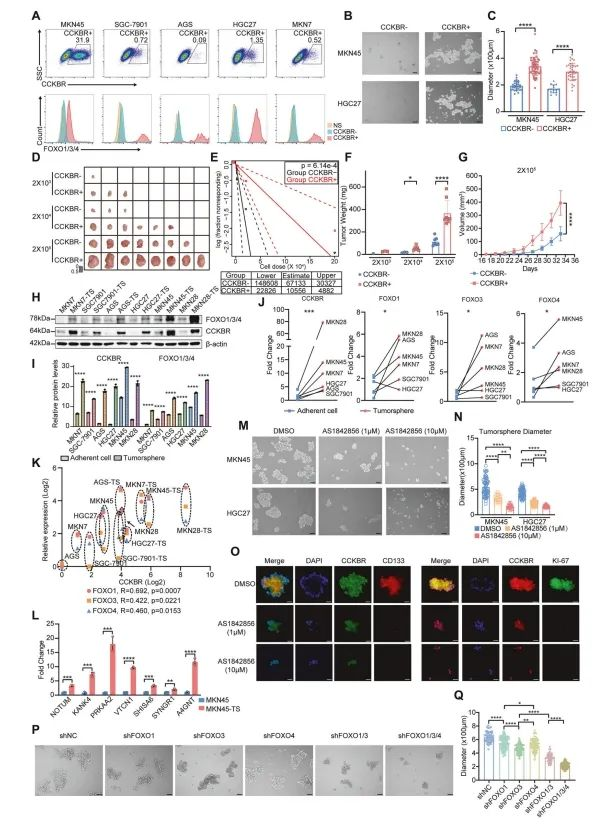
Abbildung 5. FOXO-Transkript ions faktoren behalten den stamm artigen Zustand von CCKBRs Magenkrebs zellen bei
Die Autoren unterstützten ferner die stamm artige Natur von CCKBRs-Tumorzellen und stellten fest, dass Epi5-associated Marker in von diesen Zellen abgeleiteten Tumor kugeln signifikant hoch reguliert waren (Abbildung 5L).
Um die funktionelle Rolle der FOXO-Signal übertragung zu bewerten, wurden Tumorsphären-Kulturen mit unterschied lichen Konzentrationen von AS1842856, einem selektiven FOXO-Inhibitor, behandelt. Die Behandlung mit 1 μM AS1842856 unterdrückte die Tumor kugel bildung signifikant. Darüber hinaus bestätigte die RT-qPCR-Analyse die Herunter regulierung von Wnt-Signalwegen genen, Magens tamm zell markern und CSC-Markern nach FOXO-Hemmung (ergänzende Abbildung 5E).
Um die einzelnen Beiträge von FOXO-Transkript ions faktoren zu analysieren, generierten die Autoren FOXO1-, FOXO3-und FOXO4-Knockout-Linien in MKN45-Magenkrebszellen. Einzelgen-Knockouts reduzierten nur geringfügig die Bildung von Tumors kugeln. Das doppelte Knockout von FOXO1 und FOXO3 führte jedoch zu einer deutlichen Abnahme der Kugel bildung, und das dreifache Knockout von FOXO1/3/4 führte zu einem noch größeren Hemm effekt (Abbildung 5P, 5Q).
Diese Ergebnisse legen nahe, dass kompensator ische Mechanismen zwischen FOXO-Iso formen existieren und dass eine gleichzeitige Hemmung mehrerer Mitglieder der FOXO-Familie erforderlich sein kann, um die CSC-Aktivität bei CCKBRs-Tumoren wirksam zu unterdrücken.
Um die Arzneimittel antwort zwischen CCKBRs-und CCKBRs-Tumorzellen direkt zu vergleichen, stellten die Autoren Magenkrebs-Organo ide aus Zellen mit oder ohne CCKBR-Expression fest (Abbildung 6A). In Übereinstimmung mit früheren Ergebnissen zeigten CCKBRs Organo ide eine erhöhte Expression von CCKBR-und Stamm zell markern.
Es wurde gezeigt, dass Organo ide das Arzneimittel antwort profil von Primärtumoren beibehalten. In diesem Modell unterdrückte die Behandlung mit AS1842856 das Wachstum von CCKBRs-Organo iden signifikant. Insbesondere verringerte 1 μM AS1842856 die Lebensfähig keit der Zellen, und höhere Dosen übten zytotoxische Wirkungen auf CCKBRs Magen adeno karzinom (GA)-Organo ide aus. Im Gegensatz dazu waren CCKBR-Organo ide weitgehend nicht betroffen (Abbildung 6B, 6C).
Die Autoren testeten auch Carben oxolon, einen neuartigen FOXO-Weg hemmer, der ebenfalls shSchuldete eine robuste Unterdrückung des CCKBRs GA-Organoid wachstums (Abbildung 6D).
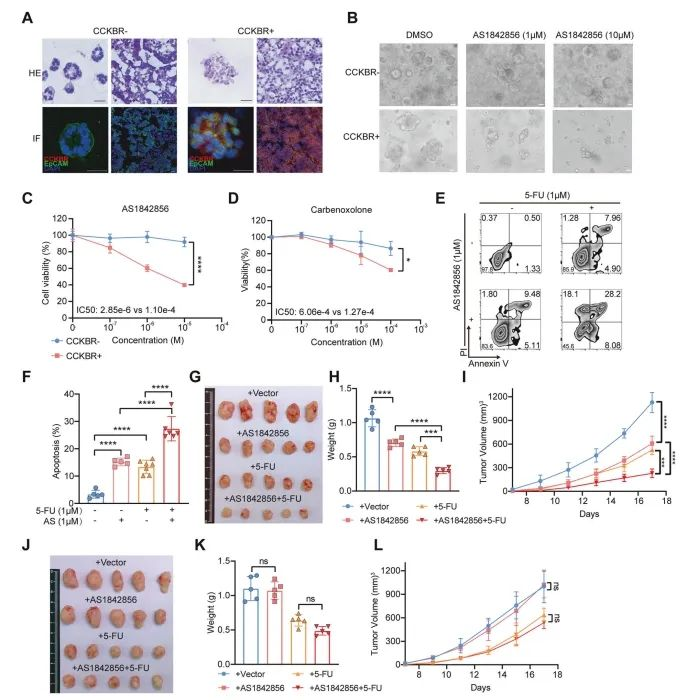
Abbildung 6. Das Targeting von FOXO unterdrückt das Wachstum von CCKBRs Tumorzellen
Zusätzlich zur Organoid hemmung untersuchten die Autoren, ob die Kombination der FOXO-Hemmung mit einer Chemo therapie die Anti tumor wirkung weiter verstärken könnte. Die Behandlung von CCKBRs-Tumorzellen mit AS1842856 und 5-Fluorouracil (5-FU) führte zu einem signifikanten Anstieg der Apoptose im Vergleich zu beiden Wirkstoffen allein (Abbildung 6E, 6F).
Um diese Kombination strategie in vivo zu bewerten, haben die Autoren CCKBRs MKN45-Zellen in immun defiziente Mäuse xeno transplant iert und sie mit AS1842856, 5-FU oder beiden behandelt. AS1842856 allein reduzierte das Tumor wachstum, während die Kombination therapie eine ausgeprägtere hemmende Wirkung auf die Tumor größe hatte (Abbildung 6G-I).
Im Gegensatz dazu hatten dieselben Behandlungen nur minimale Auswirkungen auf von AGS abgeleitete Tumoren, die CCKBR-negativ sind, was darauf hinweist, dass der therapeut ische Nutzen spezifisch für stamm ähnliche Tumorzellen von CCKBRs ist (Abbildung 6J-L).
Zusammen mit In-vitro-Ergebnissen legen diese Ergebnisse nahe, dass die FOXO-Hemmung das Wachstum von CCKBRs-Magenkrebs zellen selektiv unterdrückt, insbesondere in Kombination mit Chemo therapeutika wie 5-FU.
Um die nach gelagerten Mechanismen zu untersuchen, mit denen die FOXO-Signal übertragung CCKBRs-Tumorzellen erhält, führten die Autoren eine CUT & Tag-Sequenz ierung mit hohem Durchsatz an CCKBRs-und CCKBRs-Tumorzellen durch. Wie erwartet wurden Bindungs motive für FOXO1, FOXO3 und FOXO4 angereichert, was darauf hindeutet, dass diese Transkript ions faktoren gemeinsame regulator ische Elemente aufweisen (Abbildung 7A).
Die Differential peak analyze von Promotor regionen ergab, dass FOXO-Ziele das Überleben von Tumorzellen und die Hypoxie reaktionen förderten, was mit früheren Beobachtungen der Aktivierung des FOXO-Signalwegs in einer hypox ischen Mikro umgebung überein stimmt (Abbildung 7B).
Unter den nach geschalteten Genen war die ST3GAL-Sialyltransferase-Familie (α2, 3-Sialylierung) in CCKBRs-Zellen deutlich hoch reguliert, während Mitglieder der ST6GALNAC-Familie (α2, 6-Sialylierung) dies nicht waren. Die Aberrant-Sialylierung ist ein bekannter Treiber für Tumor progression, Met astas ierung und Immun hinterziehung.
RT-qPCR bestätigte, dass ST3GAL-Gene in CCKBRs GA-Organo iden signifikant erhöht waren und vor allem ihre Expression durch die Behandlung mit AS1842856 unterdrückt wurde (Abbildung 7I). Diese Ergebnisse wurden weiter durch MAL II-Lektin färbung validiert, die nach FOXO-Hemmung eine reduzierte α2, 3-Sialin säure zeigte (Abbildung 7J).
Schließlich führte die pharma ko logische Hemmung der α2, 3-Sialylierung unter Verwendung von P3FAX-Neu5Ac zu einer signifikanten Unterdrückung des Tumor wachstums in CCKBRs-Zellen, während sie nur minimale Auswirkungen auf CCKBR-Zellen hatte (Abbildung 7K).
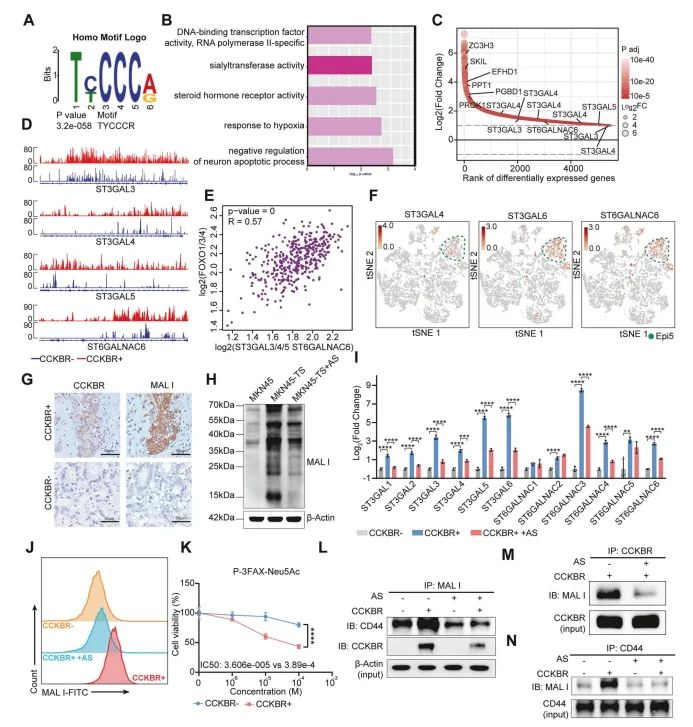
Abbildung 7. FOXOs regulieren transkript ionell die α2, 3-Sialylierung und fördern das Wachstum von CCKBRs-Tumoren
Zusammenfassend zeigt die Studie, dass FOXO-Transkript ions faktoren die Expression wichtiger Sialyl transfer asen fördern-einschl ießlich ST3GAL3, ST3GAL4, ST3GAL5 und in geringerem Maße ST6GALNAC6-in CCKBRs Magenkrebs zellen. Diese Hoch regulation führt zu erhöhten Spiegeln von α 2, 3-verknüpften Sialoglykanen an kritischen Oberflächen molekülen wie CD44 und CCKBR, fördert das Tumor wachstum und trägt möglicher weise zur Immun hinterziehung und Met astas ierung bei.
Die heterogenen Phänotypen von Magen tumoren tragen zu variablen Arzneimittel reaktionen bei und schränken letztendlich die Wirksamkeit standard isierter Behandlungs ansätze ein. In gesundem Magen gewebe spielen langlebige Stammzellen eine zentrale Rolle bei der Erhaltung des Epithels. Sowohl basale Stammzellen als auch 4 Stammzellen wurden durch zelltyp spezifische onkogene Mutationen als potenzielle Ursprungs zellen für antralen Magenkrebs in Betracht gezogen.
In dieser Studie verwendeten die Autoren die transkriptomische Profilierung einzelner Zellen, um eine CCKBR-exprimieren den 4-Stammzell-ähnlichen Sub population im distalen Magen zu identifizieren. Diese Zellen waren durch schlechte Differenzierung, hohe Malignität und Assoziation mit verringertem Überleben des Patienten gekennzeichnet.
Im Vergleich zu Tumorzellen vom Foveolar-oder Darm typ zeigten CCKBRs Krebszellen eine starke Aktivierung entzündlicher, autophagi scher und stamm assoziierter Signalwege. Die Studie ergab auch, dass FOXO SignaLeng ist wichtig, um die bösartigen und stamm artigen Eigenschaften dieses Tumors ubtyps aufrecht zu erhalten.
Darüber hinaus ident ifi zierten die Autoren eine FOXO-Sialyltransferase-Achse, die das Fortschreiten des Tumors fördert, indem sie die α 2, 3-verknüpfte Sialylierung an Oberflächen proteinen wie CD44 und CCKBR verstärkt. Erleichterung des CCKBR-gesteuerten Wachstums und Überlebens von Krebs stammzellen (Abbildung 8).
Diese Arbeit bietet neue Einblicke in die molekularen Grundlagen der Tumor hetero genität beim Magen adeno karzinom und hebt CCKBRs stamm ähnliche Tumorzellen als viel versprechen des therapeut isches Ziel hervor. Die Ausrichtung auf die FOXO-Signal übertragung und die nach gelagerten Glykosylierungs programme könnte neue Wege für Präzisions behandlungs strategien bei Magenkrebs eröffnen.
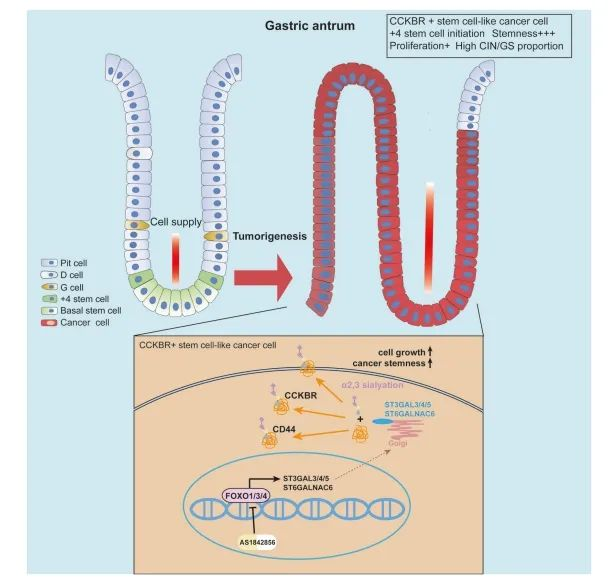
Abbildung 8. CCKBRs Krebszellen im Magen adeno karzinom weisen stamm artige Eigenschaften auf
Tan, Z., Pan, K., Sun, M. et al. CCKBR-Krebszellen tragen zur Intratumor-Hetero genität von Magenkrebs bei und verleihen eine Empfindlichkeit gegenüber FOXO-Hemmung. Zelltod unterscheiden sich 31, 1302-1317 (2024). https://doi.org/10.1038/s41418-024-01360-z
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong
Singapur Globaler Hauptsitz:112 ROBINSON ROAD #03-01
Germany: Arnold-Graffi-Haus / D85 Robert-Rössle-Straße 10 13125 Berlin
Vereinigte Staaten:2 Goddard, Irvine, CA 92618, Vereinigte Staaten
Hong Kong:Wohnung 1019B, 10/F, Liven House, Nr. 61-63 King Yip Street, Kwun Tong